Farmacología
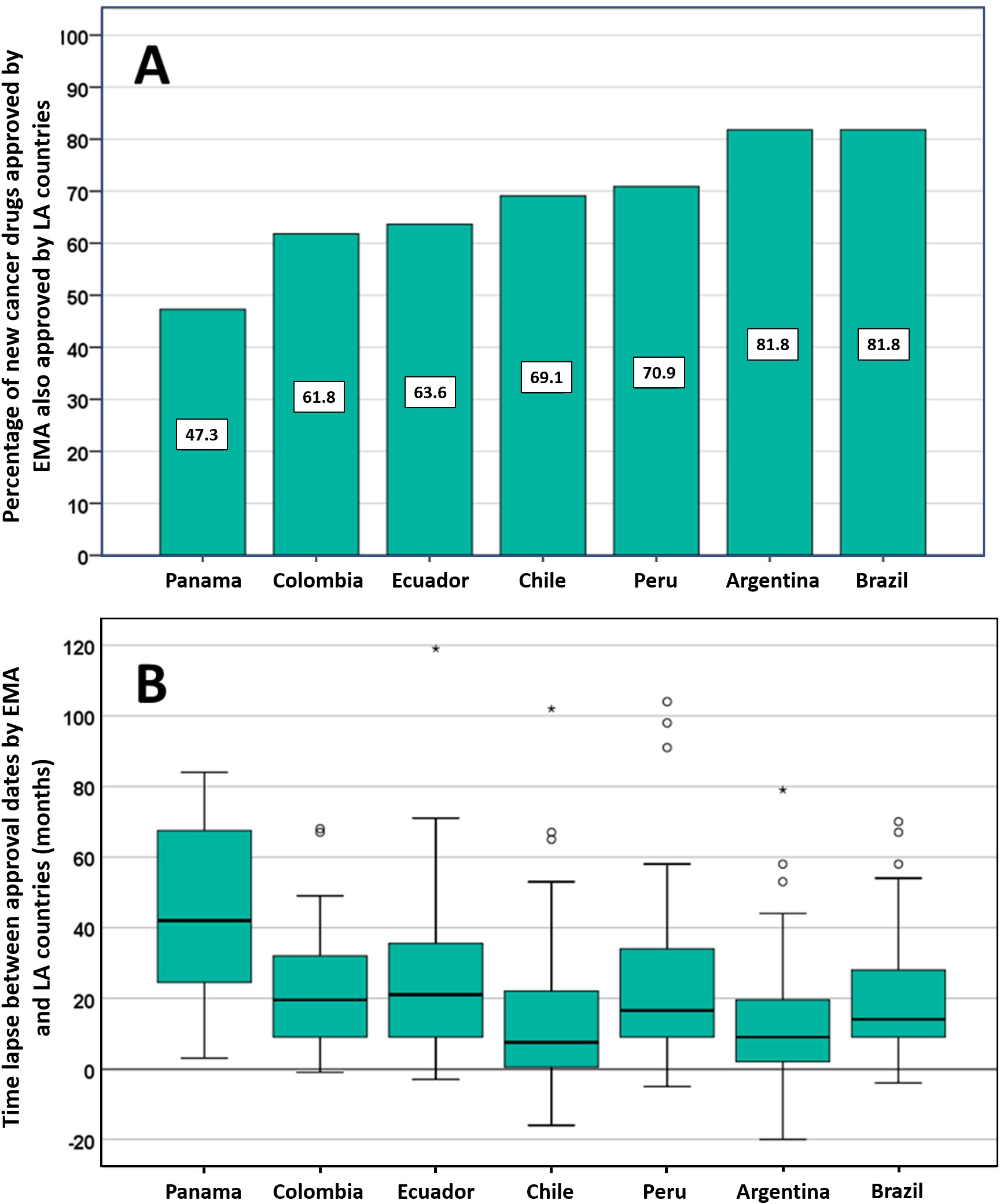
Posible impacto negativo de las decisiones de Agencias reguladoras reputadas sobre el estado de aprobación de nuevos medicamentos contra el cáncer en los países de América Latina
14 julio 2021
Los países de América Latina siguen aprobando nuevos medicamentos contra el cáncer, a menudo basándose en ensayos clínicos mal realizados que miden criterios de valoración sustitutos. La EMA y otros reguladores de renombre deben ser conscientes de que sus decisiones regulatorias pueden influir directamente en las decisiones relativas a la autorización de comercialización, los presupuestos de salud y la atención del paciente en otros lugares. PLoS ONE 13 de julio de 2021

Fortalecimiento de los sistemas regulatorios en la Región de las Américas.
28 abril 2021
Resumen de las enseñanzas obtenidas de las Autoridades Regulatorias Nacionales de referencia regional OPS/HSS/MT/21-0005. Organización Panamericana de la Salud, 26 de abril de 2021

Aprobación del real decreto por el que se regulan los estudios observacionales con medicamentos
01 diciembre 2020
El objetivo de esta nueva normativa está orientado a simplificar los procedimientos administrativos facilitando la investigación independiente, obtener una evaluación más eficiente de la calidad e idoneidad de cada estudio y actualizar las garantías de transparencia y acceso a la información de estos estudios. AEMPS 27 de noviembre de 2020

Popó de unicornio y aguas benditas: charlatanería COVID-19 y cartas de advertencia de la FDA
02 octubre 2020
Un pequeño porcentaje de las cartas de advertencia de la FDA se han centrado recientemente en COVID-19. Estas cartas exponen la charlatanería descarada y potencialmente dañina de los proveedores de todo el mundo que priorizan la ganancia financiera sobre la beneficencia clínica. La toma de antecedentes del paciente debe incluir consultas sobre productos no tradicionales y no aprobados para identificar, documentar e informar sobre charlatanería potencialmente dañina. Las cartas de advertencia de la FDA son un componente de una acción correctiva significativa; sin embargo, se necesita un mayor esfuerzo para difundir el conocimiento de tales productos tergiversados, no aprobados y adulterados para disuadir las compras de dichos productos. Ther Innov Regul Sci, 1 de octubre de 2020
Estatinas para la prevención primaria: ¿cuál es el papel del regulador?
11 marzo 2020
