Farmacología

FDA autoriza anticuerpos monoclonales (bamlanivimab y etesevimab ) juntos para el tratamiento del COVID-19
10 febrero 2021
La Administración de Medicamentos y Alimentos de EE. UU. emitió una autorización de uso de emergencia (EUA) para bamlanivimab y etesevimab administrados juntos para el tratamiento de COVID-19 leve a moderado en pacientes adultos y pediátricos (12 años de edad o más que pesen al menos 40 kilogramos ) que dan positivo al SARS-CoV-2 y que tienen un alto riesgo de progresar a COVID-19 grave. FDA , 9 de febrero de 2021

FDA autorización de emergencia del anticuerpo monoclonal bamlanivimab, para el tratamiento del COVID-19
10 noviembre 2020
La decisión se basó en un análisis intermedio de un ensayo clínico de fase II aleatorizado, doble ciego y controlado con placebo en 465 adultos no hospitalizados con síntomas de COVID-19 leves a moderados. FDA, 9 noviembre 2020

Polémica por la aprobación del remdesivir por la FDA
02 noviembre 2020
Resumimos la polémica historia del remdesivir para #Covid_19 y las implicaciones de la aprobación de comercialización de este medicamento para Latinoamérica. DIME Boletín #25, 31 de octubre de 2020

FDA aprueba por "vía rápida" remdesivir para el COVID-19, más allá de la Autorización de Uso de Emergencia
23 octubre 2020
Es el primer tratamiento aprobado por la FDA para COVID-19. Fue sobre la base de tres ensayos clínicos controlados, pero sin mención de los resultados del Ensayo SOLIDARITY en el cual no demostró resultados beneficioso sobre la mortalidad. FDA , 22 de octubre de 2020
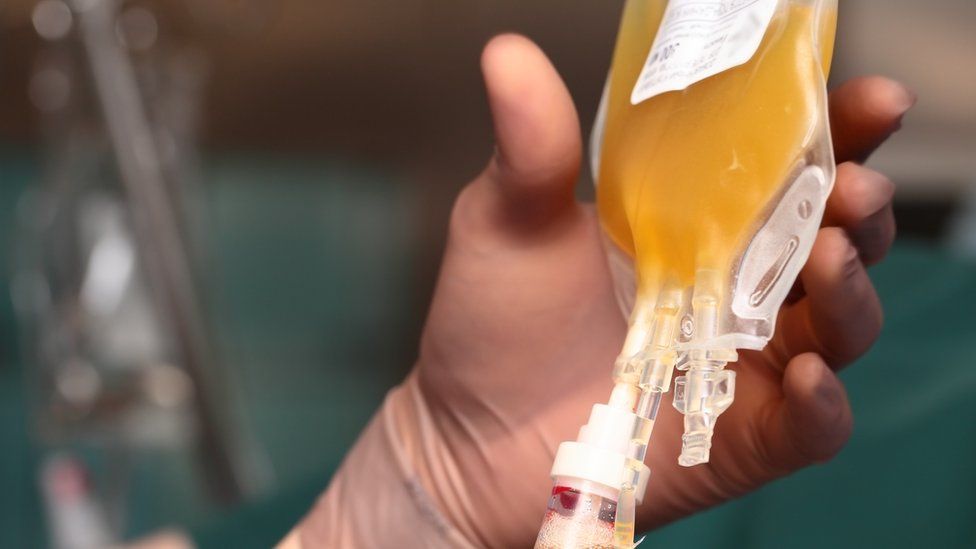
COVID-19: EE. UU. aprueba el uso de emergencia de plasma de convalecientes a pesar de las advertencias sobre la falta de pruebas
27 agosto 2020
