Farmacología

Aprobaciones de indicaciones de medicamentos contra el cáncer en China y Estados Unidos: una comparación de los tiempos de aprobación y el beneficio clínico, 2001-2020
10 abril 2024
Las indicaciones de medicamentos contra el cáncer aprobados por la FDA que demostraban un beneficio en la supervivencia tenían más probabilidades de recibir aprobaciones en China con tiempos de revisión regulatoria más cortos en comparación con las indicaciones sin dicha evidencia. Dado que los tiempos de presentación de los fabricantes fueron el principal factor de los tiempos de aprobación de medicamentos contra el cáncer en China, se deben explorar los factores que influyen en el momento de la presentación. Lancet Reg Health West Pac 1 de abril de 2024

Tiempo de revisión de los medicamentos oncológicos y sus factores subyacentes: una exploración en China
06 noviembre 2023
El breve retraso en el lanzamiento en relación con los EE. UU. fue un factor importante para la velocidad de revisión de la Administración Nacional de Productos Médicos de China, lo que podría sugerir su dependencia regulatoria latente del otro regulador global durante el período posterior a la comercialización, cuando aún faltaba nueva información sobre el beneficio clínico del medicamento. Front. Pharmacol., 1 de noviembre de 2023

Debilidad de las evidencias para la aprobación acelerada de nuevos fármacos oncológicos en China
30 agosto 2023
La mayoría de los nuevos medicamentos contra el cáncer que recibieron aprobación acelerada se basaron en tasas de respuesta en estudios sin grupo de control. Las correlaciones informadas entre los criterios de valoración subrogados y la superviviencia general (SG) fueron limitadas. Nuestros hallazgos resaltan que es esencial realizar ensayos clínicos aleatorizados y medir SG o calidad de vida para garantizar los beneficios clínicos para los pacientes. eClinicalMedicine, 24 de agosto de 2023.

Retiros de medicamentos relacionados con la seguridad en China entre 1999 y 2021
15 julio 2022
La promulgación de regulaciones y el desarrollo de sistemas pasivos y activos avanzados han mejorado la farmacovigilancia en China. Se debe fortalecer la evidencia de alta calidad, la coordinación con otras autoridades reguladoras y la comunicación y el intercambio de información para optimizar la vigilancia de la seguridad de los medicamentos y la gestión de riesgos. Drug Saf 12 de julio de 2022
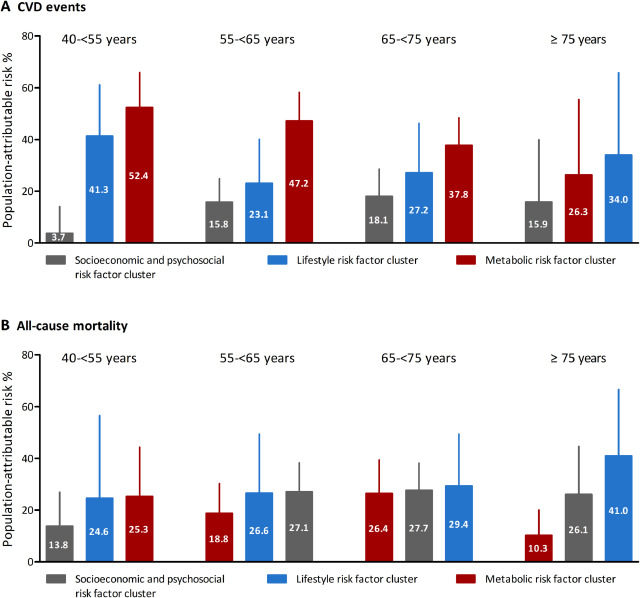
Perfiles de factores de riesgo modificables por edad para enfermedades cardiovasculares y mortalidad
29 septiembre 2021
