Farmacología
FDA solicita el retiro del mercado de todos los productos de ranitidina
01 abril 2020
FDA, 1 de abril de 2020 La FDA aconseja a los consumidores, pacientes y profesionales de la salud después de que nuevos estudios de la FDA muestran riesgos para el público
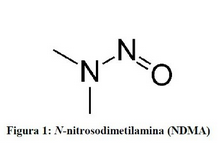
Actualización sobre las impurezas de nitrosaminas
02 enero 2020
OMS, 20 de noviembre de 2019 En julio de 2018, las autoridades sanitarias tomaron conocimiento por primera vez de la presencia de N-nitrosodimetilamina (NDMA), una impureza de nitrosamina, en productos que contenían valsartán. Este fármaco es un antagonista de los receptores de angiotensina II que pertenece a una familia de compuestos análogos denominados comúnmente sartanes. También se ha notificado también la presencia de ese tipo de impurezas en medicamentos que contienen pioglitazona y ranitidina

FDA: Los niveles de N-nitrosodimetilamina (NDMA) en ranitidina es similar a los niveles en carnes a la parrilla.
04 noviembre 2019
FDA, 1 de noviembre de 2019 FDA dice que sus recomendaciones para los pacientes permanecen sin cambios:- Aquellos que usan ranitidina o nizatidina de venta libre "pueden considerar" usar alternativas de venta libre, como famotidina u omeprazol.- Aquellos que usan ranitidina o nizatidina recetadas deben hablar con sus médicos acerca de otras opciones.

EE.UU. siguen retirando lotes de antihipertensivos por impurezas con potencial carcinógeno
07 enero 2019
