Efecto de la hidroxicloroquina sobre el estado clínico a los 14 días en pacientes hospitalizados con COVID-19. Un ensayo clínico aleatorizado
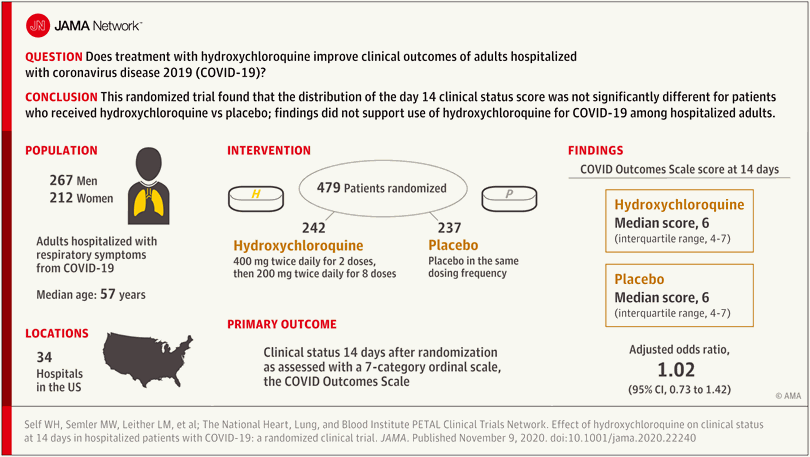
En este ensayo clínico aleatorizado que incluyó a 479 adultos hospitalizados con síntomas respiratorios de COVID-19, la distribución de la puntuación del estado clínico del día 14 (medida mediante una escala ordinal de 7 categorías) no fue significativamente diferente para los pacientes aleatorizados para recibir hidroxicloroquina en comparación con placebo (razón de posibilidades ajustada, 1,02).Estos hallazgos no apoyan el uso de hidroxicloroquina para el tratamiento de COVID-19 entre adultos hospitalizados. JAMA. 9 de noviembre de 2020
Importancia Se necesitan datos sobre la eficacia de la hidroxicloroquina para el tratamiento de la enfermedad por coronavirus 2019 (COVID-19).
Objetivo Determinar si la hidroxicloroquina es un tratamiento eficaz para los adultos hospitalizados con COVID-19.
Diseño, ámbito y participantes Este fue un ensayo aleatorio multicéntrico, ciego y controlado con placebo realizado en 34 hospitales de EE. UU. Los adultos hospitalizados con síntomas respiratorios de la infección por coronavirus 2 del síndrome respiratorio agudo severo se inscribieron entre el 2 de abril y el 19 de junio de 2020, con la última evaluación de resultados el 17 de julio de 2020. El tamaño de muestra planificado fue de 510 pacientes, con análisis provisionales planificados después de cada 102 se inscribieron pacientes. El ensayo se detuvo en el cuarto análisis intermedio por inutilidad con un tamaño de muestra de 479 pacientes.
Intervenciones Los pacientes fueron asignados aleatoriamente a hidroxicloroquina (400 mg dos veces al día para 2 dosis, luego 200 mg dos veces al día para 8 dosis) (n = 242) o placebo (n = 237).
Variables y medidas principales El resultado primario fue el estado clínico 14 días después de la aleatorización según lo evaluado con una escala ordinal de 7 categorías que van desde 1 (muerte) a 7 (dado de alta del hospital y capaz de realizar actividades normales). El resultado primario se analizó con un modelo de probabilidades proporcionales multivariable, con una razón de probabilidades ajustada (ORa) superior a 1,0 que indica resultados más favorables con hidroxicloroquina que con placebo. El ensayo incluyó 12 resultados secundarios, incluida la mortalidad a los 28 días.
Resultados Entre 479 pacientes que fueron aleatorizados (mediana de edad, 57 años; 44,3% mujeres; 37,2% hispanos / latinos; 23,4% negros; 20,1% en la unidad de cuidados intensivos; 46,8% recibieron oxígeno suplementario sin presión positiva; 11,5% recibieron ventilación no invasiva u oxígeno de alto flujo nasal; y el 6,7% recibió ventilación mecánica invasiva u oxigenación por membrana extracorpórea), 433 (90,4%) completaron la evaluación del resultado primario a los 14 días y el resto tenía el estado clínico imputado. La mediana de duración de los síntomas antes de la aleatorización fue de 5 días (rango intercuartílico [IQR], de 3 a 7 días). El estado clínico en la escala de resultado ordinal a los 14 días no difirió significativamente entre los grupos de hidroxicloroquina y placebo (puntuación media [IQR], 6 [4-7] vs 6 [4-7]; ORa, 1,02 [IC 95%, 0,73 a 1,42]). Ninguno de los 12 resultados secundarios fue significativamente diferente entre los grupos. 28 días después de la aleatorización, 25 de 241 pacientes (10,4%) en el grupo de hidroxicloroquina y 25 de 236 (10,6%) en el grupo de placebo habían muerto (diferencia absoluta, −0,2% [IC del 95%, −5,7% a 5,3% ]; ORa, 1,07 [IC del 95%, 0,54 a 2,09]).
Conclusiones y relevancia Entre los adultos hospitalizados con enfermedad respiratoria por COVID-19, el tratamiento con hidroxicloroquina, en comparación con placebo, no mejoró significativamente el estado clínico el día 14. Estos hallazgos no apoyan el uso de hidroxicloroquina para el tratamiento de COVID-19 entre adultos hospitalizados.
El ensayo
Self WH, Semler MW, Leither LM, et al. Effect of Hydroxychloroquine on Clinical Status at 14 Days in Hospitalized Patients With COVID-19: A Randomized Clinical Trial. JAMA. Published online November 09, 2020. doi:10.1001/jama.2020.22240