Eficacia de la vacuna Oxford-AstraZeneca contra el SARS-CoV-2 durante el aumento de la variante delta en India
La vacuna ChAdOx1 nCoV-19 siguió siendo eficaz contra COVID-19 de moderado a grave, incluso durante un aumento que estuvo dominado por la variante delta altamente transmisible del SARS-CoV-2. Se mantuvieron respuestas de células T específicas de picos contra la variante delta. Esta protección inmunitaria celular podría compensar la disminución de la inmunidad humoral. Lancet Infect Dis 25 de noviembre de 2021
Antecedentes: Las variantes preocupantes (COV) del SARS-CoV-2 han amenazado la eficacia de la vacuna COVID-19. Nuestro objetivo fue evaluar la eficacia de la vacuna ChAdOx1 nCoV-19 (Oxford-AstraZeneca), predominantemente contra la variante delta (B.1.617.2), además de la respuesta inmune celular a la vacunación.
Métodos: Hicimos un estudio de casos y controles con resultado negativo en dos centros de investigación médica en Faridabad, India. Todas las personas que tuvieron una prueba de RT-PCR positiva para la infección por SARS-CoV-2 entre el 1 de abril de 2021 y el 31 de mayo de 2021 se incluyeron como casos y las personas que tuvieron una prueba de RT-PCR negativa se incluyeron como controles después de la comparación con casos en la semana calendario de la prueba de RT-PCR. El resultado primario fue la efectividad de la vacunación completa con la vacuna ChAdOx1 nCoV-19 contra la infección por SARS-CoV-2 confirmada en laboratorio. Los resultados secundarios fueron la eficacia de una dosis única contra la infección por SARS-CoV-2 y la eficacia de una dosis única y la vacunación completa contra la enfermedad de moderada a grave entre las personas infectadas. Además, probamos in vitro la neutralización de virus vivos y las respuestas inmunes de células T a la proteína de pico del SARS-CoV-2 de tipo salvaje y los COV entre los receptores sanos (negativos a anticuerpos anti-nucleocápsida) de la vacuna ChAdOx1 nCoV-19.
Resultados: De 2.379 casos de infección confirmada por SARS-CoV-2, 85 (3,6%) estaban completamente vacunados en comparación con 168 (8,5%) de los 1.981 controles (OR ajustado [aOR] 0,37 [95% CI 0,28 –0,48]), dando una efectividad de la vacuna contra la infección por SARS-CoV-2 del 63,1% (95% CI 51,5–72,1). 157 (6,4%) de 2.451 de los casos y 181 (9,1%) de 1.994) controles habían recibido una dosis única de la vacuna ChAdOx1 nCoV-19 (aOR 0,54 [95% CI 0,42–0,68]), por lo que la eficacia de la vacuna de una sola dosis contra la infección por SARS-CoV-2 fue del 46,2% (IC del 95%: 31,6-57,7). Uno de los 84 casos con COVID-19 de moderado a grave estaba completamente vacunado en comparación con 84 de 2.295 casos con COVID-19 leve (ORa 0,19 [IC 95% 0,01–0,90]), lo que da una efectividad de la vacuna de vacunación completa contra la enfermedad de moderada a grave del 81,5% (IC del 95%: 9,9-99,0). La eficacia de una dosis única contra la enfermedad de moderada a grave fue del 79,2% (IC del 95%: 46,1–94,0); cuatro de 87 individuos con COVID-19 de moderado a grave habían recibido una dosis única en comparación con 153 de 2.364 participantes con enfermedad leve (ORa 0,20 [IC 95% 0,06–0,54]). Entre 49 individuos sanos, completamente vacunados, las respuestas de anticuerpos neutralizantes fueron menores contra el alfa (B.1.1.7; título medio geométrico 244,7 [IC 95% 151,8–394,4]), beta (B.1.351; 97,6 [61,2–155,8]), kappa (B.1.617.1; 112,8 [72,7–175,0]) y delta (88,4 [61,2–127,8] ) variantes que contra el SARS-CoV-2 de tipo salvaje (599,4 [376,9–953,2]). Sin embargo, las respuestas de células T CD4 y CD8 específicas de antígeno se conservaron contra la variante delta y el SARS-CoV-2 de tipo salvaje.
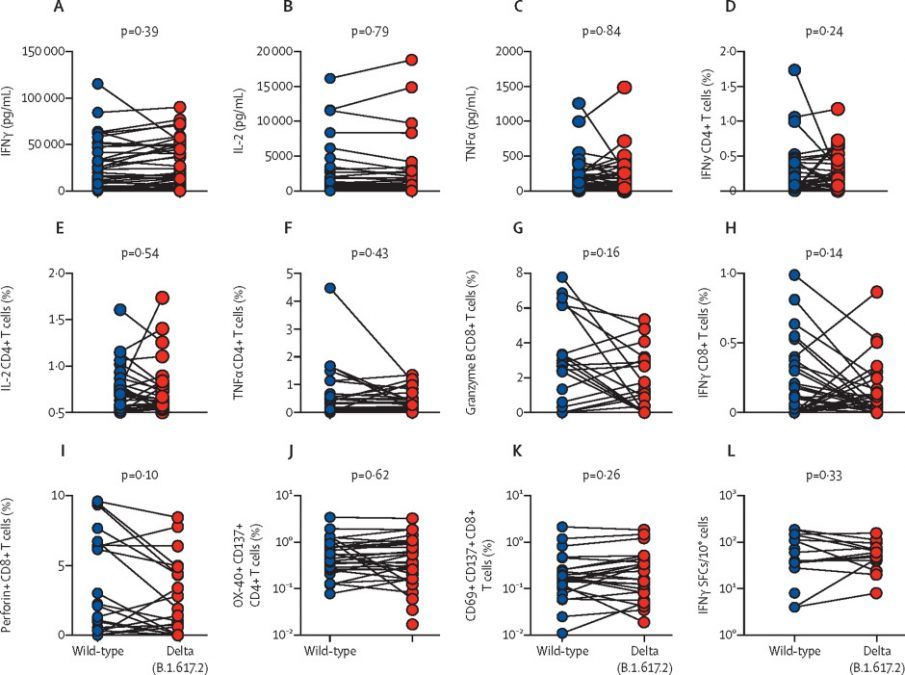
Respuestas inmunes de células T contra antígenos de pico del SARS-CoV-2 de tipo salvaje y variante delta en muestras de participantes vacunados. Concentraciones de IFNγ (A), IL-2 (B) e IFNγ (C) en el sobrenadante de cultivo de células mononucleares de sangre periférica estimuladas con grupos de péptidos de proteína de pico de tipo salvaje y variante delta durante 48 h (n = 48; 47 de 48 las muestras respondieron a la estimulación). Tinción de citocinas intracelulares para IFNγ (D), IL-2 (E) y TNFα (F) en células CD4, y granzima B (G), IFNγ (H) y perforina (I) en células CD8 estimuladas con grupos de péptidos de proteína de pico de tipo salvaje y variante delta durante 18-20 h; los gráficos muestran las proporciones de células que expresan estas moléculas (n = 41). Ensayo de marcador inducido por activación de células T CD4 (J) y células T CD8 (K) estimuladas con grupos de péptidos de proteína de pico de tipo salvaje y variante delta durante 24 h; los gráficos muestran las proporciones de células que expresan estos marcadores de activación (n = 38). (L) Activación específica de antígeno de células T por grupos de péptidos que cubren exclusivamente las regiones mutantes de la proteína de pico variante delta en comparación con el grupo de péptidos de referencia de tipo salvaje homólogo (n = 19; 19 de 24 muestras respondieron a la simulación; media 63 · 78 SFC / 106 PBMC para el tipo salvaje y 45,68 SFC / 106 PBMC para la variante delta). Cada punto de datos representa las lecturas de los pocillos estimulados por la combinación de péptidos para un participante del estudio, después de restar los pocillos estimulados con dimetilsulfóxido. IFNγ = interferón γ. SFC = células formadoras de manchas. TNFα = factor de necrosis tumoral α.
Interpretación: La vacuna ChAdOx1 nCoV-19 siguió siendo eficaz contra COVID-19 de moderado a grave, incluso durante un aumento que estuvo dominado por la variante delta altamente transmisible del SARS-CoV-2. Se mantuvieron respuestas de células T específicas de picos contra la variante delta. Esta protección inmunitaria celular podría compensar la disminución de la inmunidad humoral.
El estudio
Thiruvengadam R, Awasthi A, Medigeshi G, Bhattacharya S, Mani S, et al Department of Biotechnology India Consortium for COVID-19 research. Effectiveness of ChAdOx1 nCoV-19 vaccine against SARS-CoV-2 infection during the delta (B.1.617.2) variant surge in India: a test-negative, case-control study and a mechanistic study of post-vaccination immune responses. Lancet Infect Dis. 2021 Nov 25:S1473-3099(21)00680-0. doi: 10.1016/S1473-3099(21)00680-0.Published: November 25, 2021 DOI: 10.1016/S1473-3099(21)00680-0