Nuevos regímenes de monoterapia con benznidazol y en combinación con fosravuconazol para el tratamiento de la enfermedad de Chagas (BENDITA): un ensayo aleatorizado de fase 2, doble ciego
El benznidazol indujo una respuesta antiparasitaria eficaz, independientemente de la duración del tratamiento, la dosis o la combinación con fosravuconazol, y fue bien tolerado en pacientes adultos con enfermedad de Chagas crónica. Los regímenes más cortos o reducidos de benznidazol podrían mejorar sustancialmente la tolerabilidad y la accesibilidad al tratamiento, pero se necesitan más estudios para confirmar estos resultados. Lancet Infect Dis. 6 de abril de 2021
Antecedentes
El tratamiento actual para la enfermedad de Chagas con los únicos medicamentos disponibles, benznidazol o nifurtimox, tiene limitaciones sustanciales, incluida la duración prolongada del tratamiento y problemas de seguridad y tolerabilidad. Nuestro objetivo fue evaluar la eficacia y seguridad de nuevos regímenes de monoterapia con benznidazol y combinaciones con fosravuconazol, en el tratamiento de la enfermedad de Chagas.
Métodos
Hicimos un ensayo aleatorizado, multicéntrico, de fase 2, doble ciego, doble simulación en tres unidades ambulatorias de Bolivia. Los adultos de 18 a 50 años con enfermedad de Chagas crónica indeterminada, confirmada mediante pruebas serológicas y resultados de PCR cualitativos positivos, se asignaron al azar (1: 1: 1: 1: 1: 1: 1) a uno de siete grupos de tratamiento utilizando un bloque equilibrado esquema de aleatorización con un sistema de respuesta interactivo. Los participantes fueron asignados a benznidazol 300 mg al día durante 8 semanas, 4 semanas o 2 semanas, benznidazol 150 mg al día durante 4 semanas, benznidazol 150 mg al día durante 4 semanas más fosravuconazol, benznidazol 300 mg una vez a la semana durante 8 semanas más fosravuconazol, o placebo, con un período de seguimiento de 12 meses. Los criterios de valoración principales fueron el aclaramiento parasitológico sostenido a los 6 meses, definido como resultados de PCR cualitativos negativos persistentes desde el final del tratamiento, y la incidencia y gravedad de los eventos adversos emergentes del tratamiento, los eventos adversos graves y los eventos adversos que conducen a la interrupción del tratamiento. El análisis primario de eficacia se basó en las poblaciones por intención de tratar y por protocolo y los análisis secundarios de eficacia en la población por protocolo. Los análisis de seguridad se basaron en la población tratada. El reclutamiento ya está cerrado. Este ensayo está registrado en ClinicalTrials.gov, NCT03378661.
Resultados
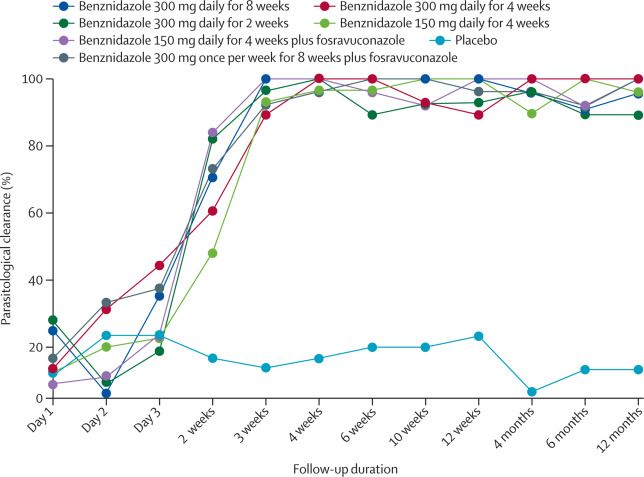
Entre el 30 de noviembre de 2016 y el 27 de julio de 2017, evaluamos a 518 pacientes y 210 se inscribieron y asignaron al azar. Se asignaron 30 pacientes (14%) a cada grupo de tratamiento. Los 210 pacientes aleatorizados se incluyeron en la población por intención de tratar y 190 (90%) en la población por protocolo. En el análisis por intención de tratar, solo uno (3%) de 30 pacientes en el grupo de placebo tuvo un aclaramiento parasitológico sostenido a los 6 meses de seguimiento. Se observó un aclaramiento parasitológico sostenido a los 6 meses en 25 (89%) de 28 pacientes que recibieron benznidazol 300 mg al día durante 8 semanas (diferencia de tasas frente a placebo 86% [IC 95% 73-99]), 25 (89%) de 28 pacientes que recibieron benznidazol 300 mg al día durante 4 semanas (86% [73-99]), 24 (83%) de 29 que recibieron benznidazol 300 mg al día durante 2 semanas (79% [64-95]), 25 (83%) de 30 que recibieron benznidazol 150 mg al día durante 4 semanas (80% [65-95]), 23 (85%) de 28 que recibieron benznidazol 150 mg al día durante 4 semanas más fosravuconazol (82% [67-97]) y 24 (83%) de 29 que recibieron benznidazol 300 mg semanales durante 8 semanas más fosravuconazol (79% [64-95]; p <0 · 0001 para todas las comparaciones de grupos con placebo). Seis pacientes (3%) tuvieron diez eventos adversos graves (leucopenia [n = 3], neutropenia [n = 2], pirexia, erupción maculopapular, colecistitis aguda, pólipo biliar y cáncer de mama), ocho tuvieron 12 eventos adversos graves (definidos como que interfiere sustancialmente con las funciones habituales del paciente; elevación de alanina aminotransferasa [n = 4], elevación de gamma-glutamiltransferasa [n = 2], elevación de aspartato aminotransferasa [n = 1], neutropenia [n = 3], leucopenia [n = 1] , y cáncer de mama [n = 1]), y 15 (7%) tuvieron eventos adversos que llevaron a la interrupción del tratamiento (la mayoría de estos fueron en los grupos que recibieron benznidazol 300 mg al día durante 8 semanas, benznidazol 300 mg una vez a la semana para 8 semanas más fosravuconazol y benznidazol 150 mg al día durante 4 semanas más fosravuconazol). No se observaron eventos adversos que llevaron a la interrupción del tratamiento en pacientes tratados con benznidazol 300 mg al día durante 2 semanas o placebo. No hubo muertes relacionadas con el tratamiento.
Interpretación
El benznidazol indujo una respuesta antiparasitaria eficaz, independientemente de la duración del tratamiento, la dosis o la combinación con fosravuconazol, y fue bien tolerado en pacientes adultos con enfermedad de Chagas crónica. Los regímenes más cortos o reducidos de benznidazol podrían mejorar sustancialmente la tolerabilidad y la accesibilidad al tratamiento, pero se necesitan más estudios para confirmar estos resultados.
El trabajo original
Torrico F, Gascón J, Barreira F, Blum B, Almeida IC, Alonso-Vega C, Barboza T, Bilbe G, Correia E, Garcia W, Ortiz L, Parrado R, Ramirez JC, Ribeiro I, Strub-Wourgaft N, Vaillant M, Sosa-Estani S; BENDITA study group. New regimens of benznidazole monotherapy and in combination with fosravuconazole for treatment of Chagas disease (BENDITA): a phase 2, double-blind, randomised trial. Lancet Infect Dis. 2021 Apr 6:S1473-3099(20)30844-6. doi: 10.1016/S1473-3099(20)30844-6.