Nuevos fármacos: ¿dónde nos hemos equivocado y como podemos mejorar?
BMJ, 10 de julio de 2019 Más de la mitad de los nuevos medicamentos en Alemania carecen de pruebas de beneficios adicionales sobre los tratamientos existentesSe debe exigir a los fabricantes que presenten datos comparativos en el momento de la aprobación del medicamento. Los pagadores podrían luego establecer el reembolso y el precio en niveles que recompensen los resultados relevantes para los pacientes
BMJ, 10 de julio de 2019
Los reguladores de medicamentos de todo el mundo están siguiendo una estrategia dirigida a acelerar el desarrollo y la aprobación de medicamentos. Estos enfoques se basan en el supuesto de que un acceso más rápido a nuevos medicamentos beneficia a los pacientes. La retórica de la novedad y la innovación crea un supuesto de que los nuevos productos son mejores que los existentes.
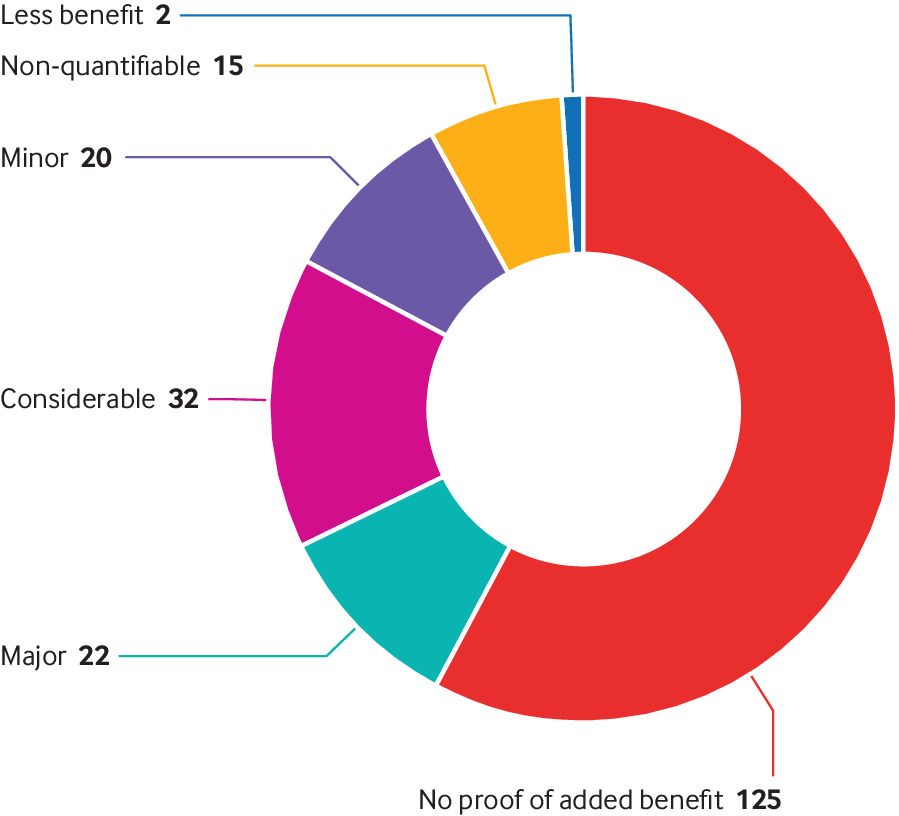
Más de la mitad de los nuevos medicamentos que ingresan al sistema de salud alemán no han demostrado tener beneficios adicionales.
Aunque sin duda existen lagunas en el arsenal terapéutico, las investigaciones que cubren las aprobaciones de medicamentos desde la década de 1970 sugieren que solo un número limitado de nuevos medicamentos proporcionan avances reales sobre los medicamentos existentes. La mayoría de los estudios consideran que la proporción de la verdadera innovación es inferior al 15%, sin una mejora clara a través del tiempo.
En este artículo Beate Wieseler y sus colegas argumentan que los procesos y políticas internacionales de desarrollo de medicamentos son responsables y deben ser reformados
En definitiva no hay evidencia de beneficio agregado para la mayoría de los medicamentos nuevos
- Más de la mitad de los nuevos medicamentos en Alemania carecen de pruebas de beneficios adicionales sobre los tratamientos existentes
- Para aumentar la innovación, se debe exigir a los fabricantes que presenten datos comparativos en el momento de la aprobación del medicamento.
- Los pagadores podrían luego establecer el reembolso y el precio en niveles que recompensen los resultados relevantes para los pacientes
- Se requiere una acción combinada a nivel nacional y de la UE para revisar el marco legal y normativo, introducir nuevos modelos de desarrollo de medicamentos y centrarse en las necesidades de los pacientes.
el artículo original
Wieseler Beate, McGauran Natalie, KaiserThomas. New drugs: where did we go wrong and what can we do better? BMJ 2019; 366:l4340
ver también