Directrices para la notificación de resultados en informes de ensayos. Extensión CONSORT-Outcomes 2022
Esta extensión CONSORT- Outcomes 2022 de la declaración CONSORT 2010 proporciona 17 elementos específicos de resultados que deben abordarse en todos los informes de ensayos clínicos publicados y puede ayudar a aumentar la utilidad, la replicabilidad y la transparencia de los ensayos y puede minimizar el riesgo de no informar selectivamente de resultados del ensayo. JAMA, 13 de diciembre de 2022
Importancia Los médicos, pacientes y legisladores confían en los resultados publicados de los ensayos clínicos para ayudar a tomar decisiones basadas en evidencia. Para evaluar críticamente y utilizar los resultados de los ensayos, los lectores necesitan información completa y transparente sobre lo que se planeó, se hizo y se encontró. Se necesita una guía específica y armonizada sobre qué información específica de resultado debe informarse en las publicaciones de ensayos clínicos para reducir las prácticas de notificación deficientes que oscurecen los problemas con la selección, evaluación y análisis de resultados.
Objetivo Desarrollar estándares armonizados, basados en evidencia y consenso para informar los resultados en informes de ensayos clínicos a través de la integración con la declaración de Estándares consolidados de informes de ensayos (CONSORT) de 2010.
Revisión de evidencia Usando el marco metodológico Mejorando la calidad y la transparencia de la investigación en salud (EQUATOR), la extensión CONSORT- Outcomes 2022 de la declaración CONSORT 2010 fue desarrollada por (1) generación y evaluación de elementos de informe de resultados candidatos a través de consultas con expertos y una revisión de alcance de orientación existente para informar los resultados de los ensayos (publicada dentro de los 10 años anteriores al 19 de marzo de 2018) identificada a través de solicitudes de expertos, búsquedas en bases de datos electrónicas de MEDLINE y el Registro Metodológico Cochrane, búsquedas en literatura gris y búsquedas en listas de referencias; (2) un proceso de votación internacional Delphi de 3 rondas (noviembre de 2018 a febrero de 2019) completado por 124 panelistas de 22 países para calificar e identificar elementos adicionales; y (3) una reunión de consenso en persona (9 y 10 de abril de
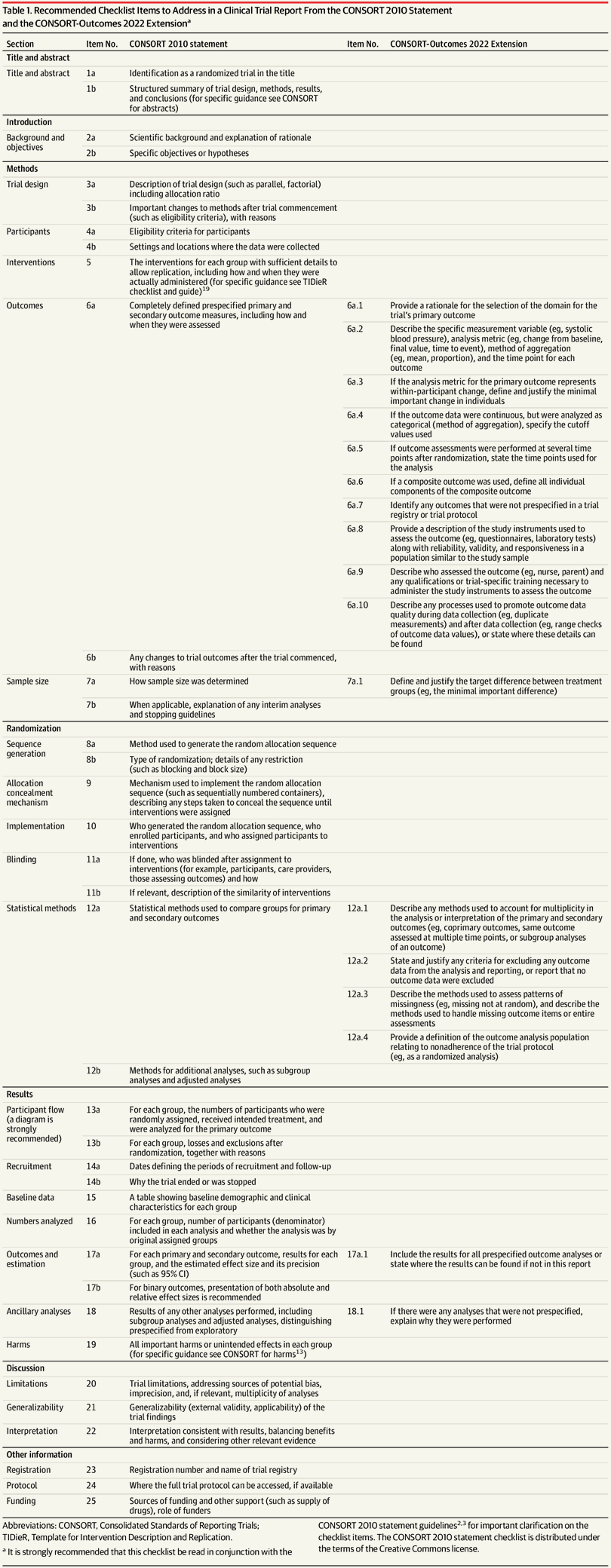
Hallazgos La revisión panorámica y la consulta con expertos identificaron 128 recomendaciones relevantes para informar los resultados en los informes de los ensayos, la mayoría (83 %) de las cuales no se incluyeron en la declaración CONSORT 2010. Todas las recomendaciones se consolidaron en 64 elementos para la votación de Delphi; después del proceso de encuesta Delphi, 30 artículos cumplieron con los criterios para una evaluación adicional en la reunión de consenso y una posible inclusión en la extensión CONSORT-Outcomes 2022. Las discusiones durante y después de la reunión de consenso produjeron 17 elementos que elaboran los elementos de la lista de verificación de la declaración CONSORT 2010 y están relacionados con la definición y justificación completas de los resultados del ensayo, incluido cómo y cuándo se evaluaron (punto 6a de la lista de verificación de la declaración CONSORT 2010),
Conclusiones y relevancia Esta extensión CONSORT- Outcomes 2022 de la declaración CONSORT 2010 proporciona 17 elementos específicos de resultados que deben abordarse en todos los informes de ensayos clínicos publicados y puede ayudar a aumentar la utilidad, la replicabilidad y la transparencia de los ensayos y puede minimizar el riesgo de no informar selectivamente de resultados del ensayo.
La guía
Butcher NJ, Monsour A, Mew EJ, et al. Guidelines for Reporting Outcomes in Trial Reports: The CONSORT-Outcomes 2022 Extension. JAMA. 2022;328(22):2252–2264. doi:10.1001/jama.2022.21022