Cobertura mediática de las advertencias de seguridad de las agencias reguladoras de medicamentos: un estudio de caso de citalopram y denosumab.
Se encontró una cobertura mediática limitada de los daños resaltados en las advertencias de seguridad. Casi dos tercios de las historias de los medios sobre denosumab no incluyeron ninguna información sobre daños, a pesar de las numerosas advertencias durante este período de tiempo. La cobertura de citalopram cubrió los daños con mayor frecuencia pero rara vez mencionó arritmias cardíacas. Estos hallazgos plantean interrogantes sobre cómo garantizar que las comunicaciones regulatorias de riesgo lleguen mejor al público en general. Br J Clin Pharmacol. 17 de febrero de 2020
Objetivos
Los reguladores de medicamentos emiten advertencias de seguridad para advertir a los médicos y al público sobre nuevas pruebas de los efectos nocivos de los medicamentos. No está claro con qué frecuencia los medios cubren estos mensajes. Nuestro objetivo fue analizar el alcance de la cobertura mediática de dos medicamentos sujetos a advertencias de seguridad desde 2007 hasta 2016 en Australia, Canadá, Reino Unido y Estados Unidos.
Métodos:
Se seleccionaron dos medicamentos ampliamente utilizados para tratar la salud mental o las condiciones físicas: citalopram y denosumab. Los informes de los medios se identificaron mediante la búsqueda de LexisNexis y Factiva. Los informes se incluyeron si indicaban al menos un beneficio o daño para la salud. Se realizó un análisis de contenido de los informes.
Resultados
En total, se incluyeron 195 informes de los medios sobre citalopram y 239 sobre denosumab. Para el citalopram, 43.1% (84/195) de los informes mencionaron beneficios, 85.6% (167/195) mencionaron daños y 9.7% (19/195) mencionaron el daño descrito en los avisos (arritmia cardíaca). Para el denosumab, el 94.1% (225/239) de los informes mencionaron beneficios y el 39.7% (95/239) mencionaron daños. Los daños descritos en los avisos rara vez se mencionaron: 10.9% (26/239) de los informes mencionaron osteonecrosis y ≤5% mencionaron cualquiera de los otros daños (fracturas atípicas, hipocalcemia, infecciones graves y reacciones dermatológicas).
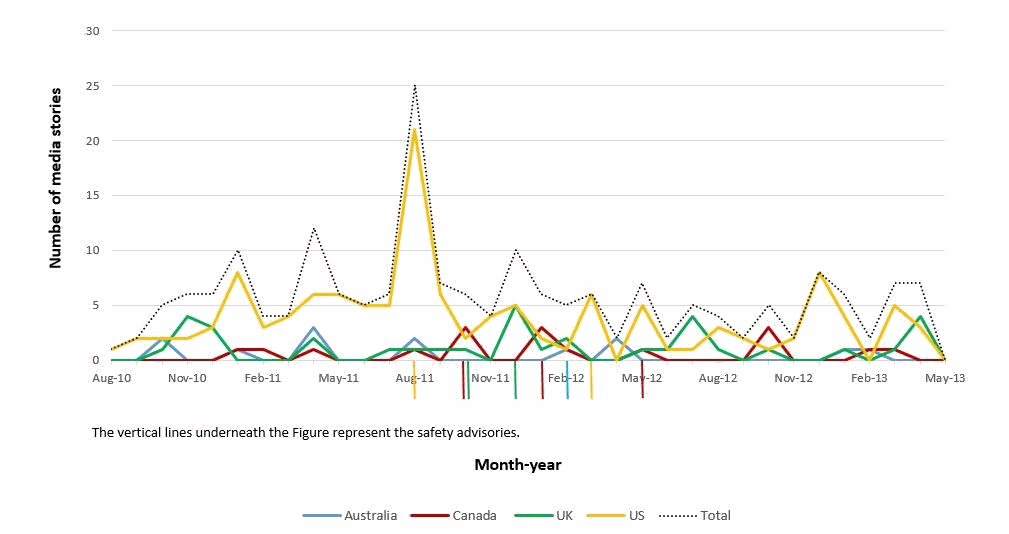
Figure 3. Number of media reports on Citalopram per month
Figure 5. Number of media reports on Denosumab per month
Conclusiones
Encontramos una cobertura mediática limitada de los daños resaltados en las advertencias de seguridad. Casi dos tercios de las historias de los medios sobre denosumab no incluyeron ninguna información sobre daños, a pesar de las numerosas advertencias durante este período de tiempo. La cobertura de citalopram cubrió los daños con mayor frecuencia pero rara vez mencionó arritmias cardíacas. Estos hallazgos plantean interrogantes sobre cómo garantizar que las comunicaciones regulatorias de riesgo lleguen mejor al público en general.
el articulo
Fabbri A, O'Keeffe M, Moynihan R, Møllebaek M, Mohammad A, Bhasale A, Puil L, Mintzes B Media coverage of drug regulatory agencies' safety advisories: a case study of citalopram and denosumab. Br J Clin Pharmacol. 2020 Feb 17. doi: 10.1111/bcp.14255. [Epub ahead of print]