Evolución del ensayo clínico aleatorizado en la era de la oncología de precisión
Este estudio de cohorte sugiere que los ECA oncológicos contemporáneos ahora miden en gran medida las variables de desenlace principales subrogadas y están financiados casi exclusivamente por la industria farmacéutica. El papel cada vez más importante de los escritores médicos merece atención. Para demostrar que los nuevos tratamientos contra el cáncer son de gran valor, la comunidad oncológica debe considerar hasta qué punto las variables de desenlace principales del estudio y el tamaño del efecto objetivo proporcionan un beneficio significativo a los pacientes. JAMA Oncol, 25 de marzo de 2021
Puntos clave
Pregunta ¿Cuáles son las características que definen los ensayos clínicos aleatorios (ECA) modernos en oncología? ¿Se diferencian de las características de los ECA de las décadas anteriores?
Hallazgos En este estudio de cohorte de 298 ECA, la supervivencia libre de progresión fue el criterio de valoración predominante de los ECA oncológicos, y las ganancias medias de supervivencia siguen siendo modestas. Casi todos los ECA ahora están financiados por la industria; esto va acompañado de un aumento sustancial en el uso de escritores médicos profesionales.
Significado La comunidad oncológica debe considerar nuevos enfoques para el diseño del estudio para garantizar que los tratamientos ofrezcan importantes beneficios a los pacientes; Paralelamente, el modelo actual de financiación de los ensayos clínicos sobre el cáncer requiere una atención urgente.
Resumen
Importancia El ensayo clínico aleatorizado (ECA) en oncología ha evolucionado desde su adopción generalizada en la década de 1970. En los últimos años, han surgido preocupaciones con respecto al uso de criterios de valoración supuestos sustitutos, como la supervivencia libre de progresión (SLP) y los tamaños del efecto marginal.
Objetivo Describir las tendencias contemporáneas en ECA oncológicos y comparar estos hallazgos con eras anteriores de diseño y producción de ECA.
Diseño, ámbito y participantes Estudio de cohorte retrospectivo de ECA de terapia sistémica en cáncer de mama, colorrectal y de pulmón de células no pequeñas publicados en 7 revistas importantes entre 2010 y 2020. Esta estrategia reproduce trabajos anteriores y permite comparar las tendencias con ECA publicados entre 1995 a 2004 y 2005 a 2009.
Variables de desenlace principales Los datos sobre el diseño, la financiación, los resultados y el informe de los ECA se extrajeron del informe de ECA publicado. Los resultados del período actual (2010-2020) se compararon con los datos de los ECA publicados entre 1995 y 2004 y entre 2005 y 2009. Se utilizaron estadísticas descriptivas y bivariadas para analizar las tendencias temporales.
Resultados La cohorte incluyó 298 ECA (132 [44%] de mama, 111 [37%] de cáncer de pulmón de células no pequeñas, 55 [19%] de cáncer colorrectal). El tratamiento experimental incluyó terapias con inhibidores moleculares (171 de 298 [57%]), citotóxicas (83 de 298 [28%]), hormonales (15 de 298 [5%]) e inmunes (24 de 298 [8%]). El sesenta y nueve por ciento (206 de 298) de los ECA fueron de intención paliativa. El criterio de valoración principal más común ahora es la SLP; esto ha aumentado sustancialmente con el tiempo (del 0% [0 de 167] al 18% [25 de 137] al 42% [125 de 298]; P <0,001). De 298 ECA, 265 (89%) ahora están financiados por la industria (anteriormente 95 de 167 [57%] y 107 de 137 [78%]; P <0,001). El cincuenta y ocho por ciento (173 de 298) de los ensayos alcanzaron su criterio de valoración principal. Entre los ensayos positivos, la mejora media en la supervivencia general y la SLP fue de 3,4 y 2,9 meses, respectivamente. Más de un tercio (117 de 298 [39%]) de los informes utilizaron un redactor médico profesional; esto aumentó sustancialmente durante el período de estudio (de 3 de 27 [11%] en 2010 a 12 de 18 [67%] en 2020; P <0,001).
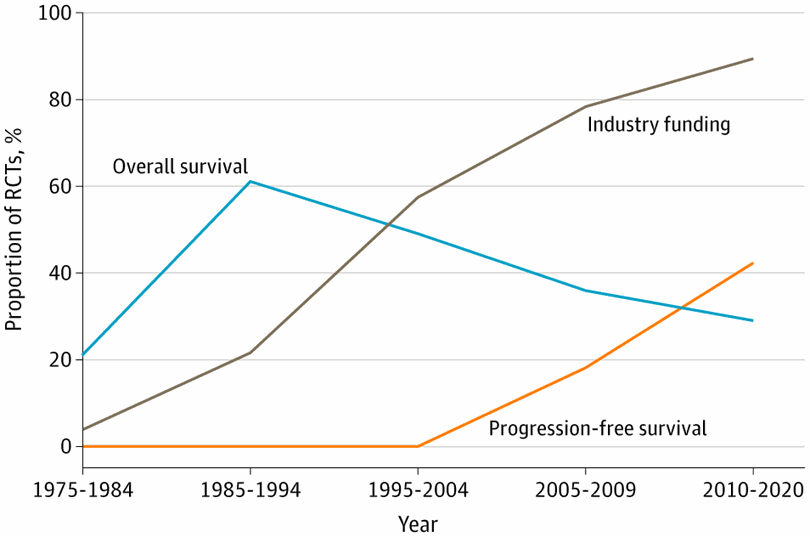
Figura 2. Tendencias temporales en el criterio principal de valoración y la financiación de la industria de ensayos clínicos aleatorizados (ECA) de cáncer de mama, colorrectal y de pulmón de células no pequeñas publicados en las principales revistas durante 5 décadas, 1975-2020
Conclusiones y relevancia Este estudio de cohorte sugiere que los ECA oncológicos contemporáneos ahora miden en gran medida los puntos finales subrogados putativos y están financiados casi exclusivamente por la industria farmacéutica. El papel cada vez más importante de los escritores médicos merece atención. Para demostrar que los nuevos tratamientos contra el cáncer son de gran valor, la comunidad oncológica debe considerar hasta qué punto las variables de desenlace principales del estudio y el tamaño del efecto objetivo proporcionan un beneficio significativo a los pacientes.
El trabajo original
Del Paggio JC, Berry JS, Hopman WM, et al. Evolution of the Randomized Clinical Trial in the Era of Precision Oncology. JAMA Oncol. Published online March 25, 2021. doi:10.1001/jamaoncol.2021.0379
Evolución del ensayo clínico aleatorizado en la era de la oncología de precisión
JAMA Oncol, 25 de marzo de 2021
Puntos clave
Pregunta ¿Cuáles son las características que definen los ensayos clínicos aleatorios (ECA) modernos en oncología? ¿Se diferencian de las características de los ECA de las décadas anteriores?
Hallazgos En este estudio de cohorte de 298 ECA, la supervivencia libre de progresión fue el criterio de valoración predominante de los ECA oncológicos, y las ganancias medias de supervivencia siguen siendo modestas. Casi todos los ECA ahora están financiados por la industria; esto va acompañado de un aumento sustancial en el uso de escritores médicos profesionales.
Significado La comunidad oncológica debe considerar nuevos enfoques para el diseño del estudio para garantizar que los tratamientos ofrezcan importantes beneficios a los pacientes; Paralelamente, el modelo actual de financiación de los ensayos clínicos sobre el cáncer requiere una atención urgente.
Resumen
Importancia El ensayo clínico aleatorizado (ECA) en oncología ha evolucionado desde su adopción generalizada en la década de 1970. En los últimos años, han surgido preocupaciones con respecto al uso de criterios de valoración supuestos sustitutos, como la supervivencia libre de progresión (SLP) y los tamaños del efecto marginal.
Objetivo Describir las tendencias contemporáneas en ECA oncológicos y comparar estos hallazgos con eras anteriores de diseño y producción de ECA.
Diseño, ámbito y participantes Estudio de cohorte retrospectivo de ECA de terapia sistémica en cáncer de mama, colorrectal y de pulmón de células no pequeñas publicados en 7 revistas importantes entre 2010 y 2020. Esta estrategia reproduce trabajos anteriores y permite comparar las tendencias con ECA publicados entre 1995 a 2004 y 2005 a 2009.
Variables de desenlace principales Los datos sobre el diseño, la financiación, los resultados y el informe de los ECA se extrajeron del informe de ECA publicado. Los resultados del período actual (2010-2020) se compararon con los datos de los ECA publicados entre 1995 y 2004 y entre 2005 y 2009. Se utilizaron estadísticas descriptivas y bivariadas para analizar las tendencias temporales.
Resultados La cohorte incluyó 298 ECA (132 [44%] de mama, 111 [37%] de cáncer de pulmón de células no pequeñas, 55 [19%] de cáncer colorrectal). El tratamiento experimental incluyó terapias con inhibidores moleculares (171 de 298 [57%]), citotóxicas (83 de 298 [28%]), hormonales (15 de 298 [5%]) e inmunes (24 de 298 [8%]). El sesenta y nueve por ciento (206 de 298) de los ECA fueron de intención paliativa. El criterio de valoración principal más común ahora es la SLP; esto ha aumentado sustancialmente con el tiempo (del 0% [0 de 167] al 18% [25 de 137] al 42% [125 de 298]; P <0,001). De 298 ECA, 265 (89%) ahora están financiados por la industria (anteriormente 95 de 167 [57%] y 107 de 137 [78%]; P <0,001). El cincuenta y ocho por ciento (173 de 298) de los ensayos alcanzaron su criterio de valoración principal. Entre los ensayos positivos, la mejora media en la supervivencia general y la SLP fue de 3,4 y 2,9 meses, respectivamente. Más de un tercio (117 de 298 [39%]) de los informes utilizaron un redactor médico profesional; esto aumentó sustancialmente durante el período de estudio (de 3 de 27 [11%] en 2010 a 12 de 18 [67%] en 2020; P <0,001).
Conclusiones y relevancia
Evolución del ensayo clínico aleatorizado en la era de la oncología de precisión
JAMA Oncol, 25 de marzo de 2021
Puntos clave
Pregunta ¿Cuáles son las características que definen los ensayos clínicos aleatorios (ECA) modernos en oncología? ¿Se diferencian de las características de los ECA de las décadas anteriores?
Hallazgos En este estudio de cohorte de 298 ECA, la supervivencia libre de progresión fue el criterio de valoración predominante de los ECA oncológicos, y las ganancias medias de supervivencia siguen siendo modestas. Casi todos los ECA ahora están financiados por la industria; esto va acompañado de un aumento sustancial en el uso de escritores médicos profesionales.
Significado La comunidad oncológica debe considerar nuevos enfoques para el diseño del estudio para garantizar que los tratamientos ofrezcan importantes beneficios a los pacientes; Paralelamente, el modelo actual de financiación de los ensayos clínicos sobre el cáncer requiere una atención urgente.
Resumen
Importancia El ensayo clínico aleatorizado (ECA) en oncología ha evolucionado desde su adopción generalizada en la década de 1970. En los últimos años, han surgido preocupaciones con respecto al uso de criterios de valoración supuestos sustitutos, como la supervivencia libre de progresión (SLP) y los tamaños del efecto marginal.
Objetivo Describir las tendencias contemporáneas en ECA oncológicos y comparar estos hallazgos con eras anteriores de diseño y producción de ECA.
Diseño, ámbito y participantes Estudio de cohorte retrospectivo de ECA de terapia sistémica en cáncer de mama, colorrectal y de pulmón de células no pequeñas publicados en 7 revistas importantes entre 2010 y 2020. Esta estrategia reproduce trabajos anteriores y permite comparar las tendencias con ECA publicados entre 1995 a 2004 y 2005 a 2009.
Variables de desenlace principales Los datos sobre el diseño, la financiación, los resultados y el informe de los ECA se extrajeron del informe de ECA publicado. Los resultados del período actual (2010-2020) se compararon con los datos de los ECA publicados entre 1995 y 2004 y entre 2005 y 2009. Se utilizaron estadísticas descriptivas y bivariadas para analizar las tendencias temporales.
Resultados La cohorte incluyó 298 ECA (132 [44%] de mama, 111 [37%] de cáncer de pulmón de células no pequeñas, 55 [19%] de cáncer colorrectal). El tratamiento experimental incluyó terapias con inhibidores moleculares (171 de 298 [57%]), citotóxicas (83 de 298 [28%]), hormonales (15 de 298 [5%]) e inmunes (24 de 298 [8%]). El sesenta y nueve por ciento (206 de 298) de los ECA fueron de intención paliativa. El criterio de valoración principal más común ahora es la SLP; esto ha aumentado sustancialmente con el tiempo (del 0% [0 de 167] al 18% [25 de 137] al 42% [125 de 298]; P <0,001). De 298 ECA, 265 (89%) ahora están financiados por la industria (anteriormente 95 de 167 [57%] y 107 de 137 [78%]; P <0,001). El cincuenta y ocho por ciento (173 de 298) de los ensayos alcanzaron su criterio de valoración principal. Entre los ensayos positivos, la mejora media en la supervivencia general y la SLP fue de 3,4 y 2,9 meses, respectivamente. Más de un tercio (117 de 298 [39%]) de los informes utilizaron un redactor médico profesional; esto aumentó sustancialmente durante el período de estudio (de 3 de 27 [11%] en 2010 a 12 de 18 [67%] en 2020; P <0,001).
Conclusiones y relevancia Este estudio de cohorte sugiere que los ECA oncológicos contemporáneos ahora miden en gran medida los puntos finales subrogados putativos y están financiados casi exclusivamente por la industria farmacéutica. El papel cada vez más importante de los escritores médicos merece atención. Para demostrar que los nuevos tratamientos contra el cáncer son de gran valor, la comunidad oncológica debe considerar hasta qué punto las variables de desenlace principales del estudio y el tamaño del efecto objetivo proporcionan un beneficio significativo a los pacientes.
El trabajo original
Del Paggio JC, Berry JS, Hopman WM, et al. Evolution of the Randomized Clinical Trial in the Era of Precision Oncology. JAMA Oncol. Published online March 25, 2021. doi:10.1001/jamaoncol.2021.0379
El trabajo original
Del Paggio JC, Berry JS, Hopman WM, et al. Evolution of the Randomized Clinical Trial in the Era of Precision Oncology. JAMA Oncol. Published online March 25, 2021. doi:10.1001/jamaoncol.2021.0379