Farmacología

FDA alerta a los pacientes y profesionales de atención médica acerca de los hallazgos de impurezas de nitrosamina en ciertos productos de metformina de liberación prolongada
01 junio 2020
La Administración de Alimentos y Medicamentos de los EE.UU. (FDA, en inglés) anunció que pruebas realizadas por el laboratorio de la agencia han mostrado niveles de impureza de nitrosamina, N-nitrosodimetilamina, (NDMA, por sus siglas en inglés) superiores al límite aceptable de ingesta de la agencia en varios lotes de la formulación de metformina de liberación prolongada (ER, por sus siglas en ingles), un medicamento para pacientes con diabetes tipo 2.FDA 28 de mayo de 2020
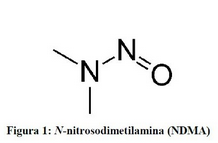
Actualización sobre las impurezas de nitrosaminas
02 enero 2020
OMS, 20 de noviembre de 2019 En julio de 2018, las autoridades sanitarias tomaron conocimiento por primera vez de la presencia de N-nitrosodimetilamina (NDMA), una impureza de nitrosamina, en productos que contenían valsartán. Este fármaco es un antagonista de los receptores de angiotensina II que pertenece a una familia de compuestos análogos denominados comúnmente sartanes. También se ha notificado también la presencia de ese tipo de impurezas en medicamentos que contienen pioglitazona y ranitidina

Información sobre la detección de nitrosaminas en medicamentos con metformina
06 diciembre 2019
AEMPS, 6 de diciembre de 2019La AEMPS informa de la detección de nitrosaminas en algunos lotes de medicamentos que contienen metformina. La Agencias europeas trabajan para evaluar las implicaciones de este hallazgo. Mientras concluye esta evaluación, la AEMPS informa a profesionales sanitarios y pacientes que actualmente no hay justificación para suspender los tratamientos con metformina.

ANMAT no retira productos con ranitidina
04 octubre 2019
