Farmacología

La EMA recomienda la autorización de la primera vacuna frente a la COVID-19
22 diciembre 2020
Comirnaty es el nombre de la vacuna desarrollada por BioNTech y Pfizer, que previne la enfermedad causada por SARS-CoV-2 en personas a partir de los 16 añosEl CHMP, formado por expertos de las autoridades competentes, entre ellas la AEMPS, ha completado su evaluación científica concluyendo por consenso que el balance beneficio-riesgo es positivo y se dispone de datos suficientemente sólidos sobre la calidad, seguridad y eficacia de esta vacunaAllana así el camino para que la Comisión Europea otorgue la autorización de comercialización condicional al medicamento y se convierta en la primera vacuna autorizada la Unión EuropeaEl ensayo clínico ha contado con la participación de unas 44.000 personas y ha demostrado una eficacia del 95%. AEMPS, 21 de diciembre de 2020
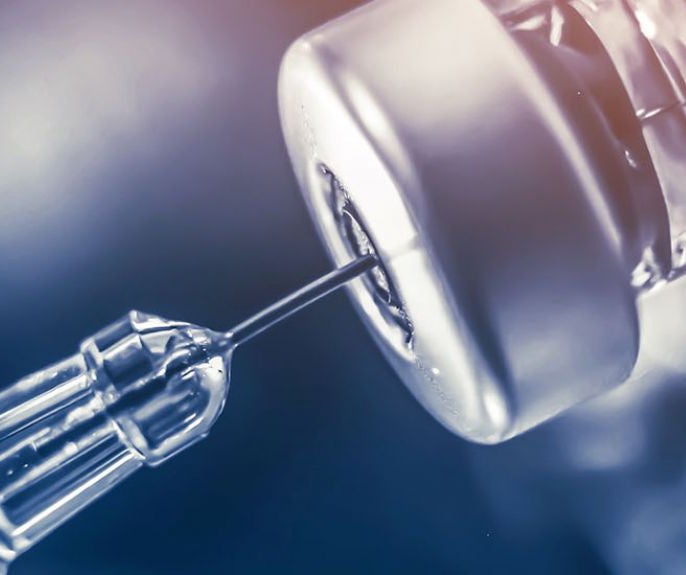
BioNTech y Pfizer publican datos intermedios de eficacia de su vacuna contra la COVID-19
10 noviembre 2020
La compañía ha comunicado datos preliminares extraídos del ensayo clínico en fase III que todavía sigue su curso. Los resultados resultan prometedores con un 90% de eficacia vacunal.El ensayo evalúa la eficacia de la vacuna administrando vacuna o placebo a los voluntarios y monitorizando e identificando cuántos positivos se producen en COVID-19.Es necesario esperar a que el ensayo finalice para poder obtener todos los datos y establecer conclusiones sólidas.La EMA empezó el proceso “rolling review” de esta vacuna el pasado 6 de octubre, pero la evaluación formal de los datos de eficacia todavía no ha comenzado.Hasta que no se haya efectuado una evaluación formal de todos los datos no se podrán extraer conclusiones, pero los resultados son esperanzadores. AEMPS, 10 de noviembre de 2020
España: Recomendaciones para el tratamiento con remdesivir de pacientes con COVID-19
29 julio 2020
La Agencia recomienda priorizar el uso de remdesivir para tratamientos con una duración máxima de 5 días en pacientes con COVID-19 hospitalizados que requieran oxigeno suplementario, pero no ventilación mecánica u oxigenación por membrana extracorpórea (ECMO) AEMPS, 28 de julio de 2020
AEMPS toma medidas con respecto a los ensayos clínicos para la COVID-19 con hidroxicloroquina
24 junio 2020
Ante recientes resultados, la AEMPS ha decidido implementar acciones para los 20 ensayos autorizados en España con este medicamento.Se suspende el reclutamiento en los brazos de hidroxicloroquina en aquellos ensayos que incluyen una población similar a los estudios RECOVERY y SOLIDARITY o en profilaxis post-exposición por ausencia de eficacia.Se mantiene el reclutamiento en los estudios que pueden generar evidencia adicional sobre la utilidad de este medicamento en el manejo de la COVID-19. AEMPS, 22 de junio de 2020
Resistencia bacteriana y COVID-19, recomendaciones para el uso prudente de los antibióticos durante la pandemia
27 mayo 2020
