Farmacología
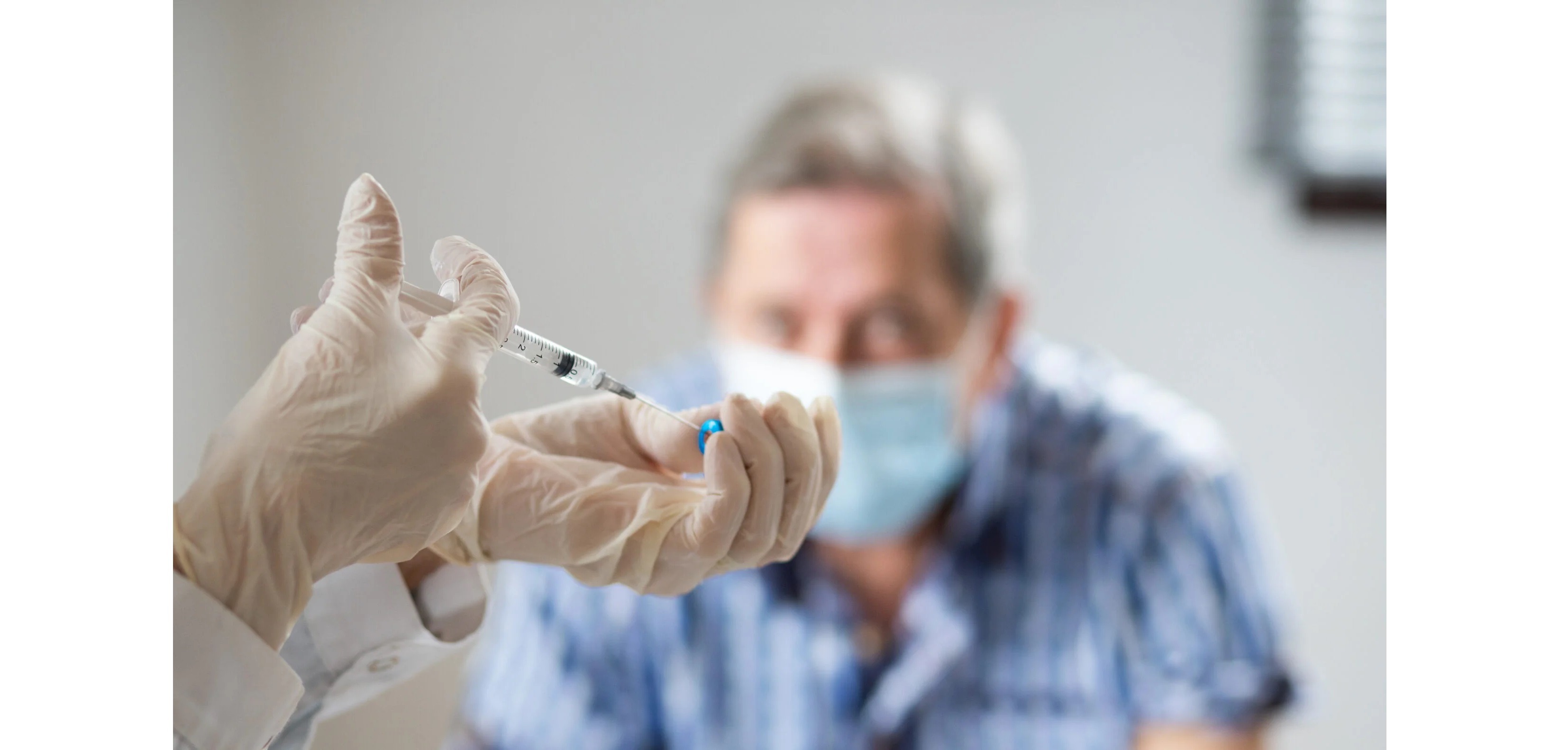
Efectividad y riesgos de las vacunas contra el virus sincicial respiratorio en adultos sin embarazo ni inmunodepresión
04 marzo 2026
Las vacunas de subunidades proteicas contra el virus sincicial respiratorio reducen el riesgo de hospitalización y enfermedad grave en adultos mayores. Annals of Internal Medicine, marzo de 2026.
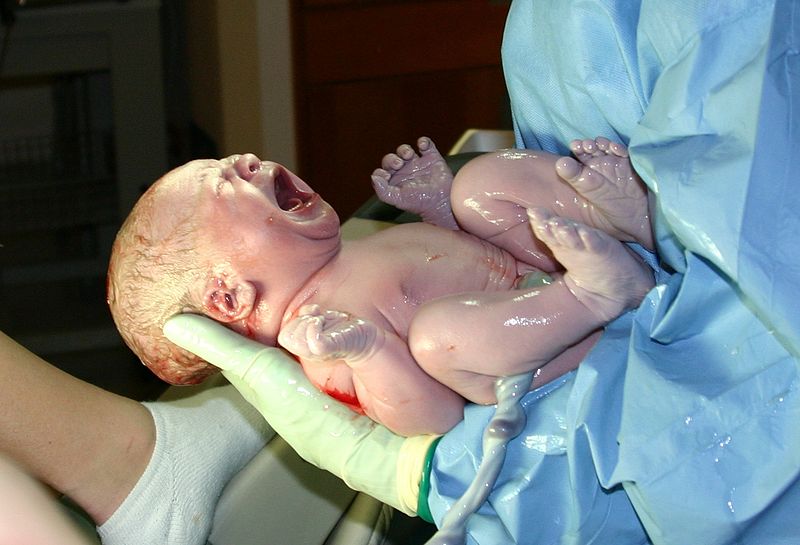
Nirsevimab vs vacuna RSVpreF y hospitalización relacionada con el virus respiratorio sincicial en recién nacidos
05 enero 2026
En comparación con la vacunación materna con la vacuna RSVpreF, la inmunización infantil pasiva con nirsevimab se asoció con un menor riesgo de hospitalización relacionada con el VRS y desenlaces graves. Estos hallazgos reflejan la primera temporada de VRS con el uso de estas estrategias de inmunización en Francia continental; su uso debería reevaluarse en futuros estudios. JAMA, 22 de diciembre de 2025.
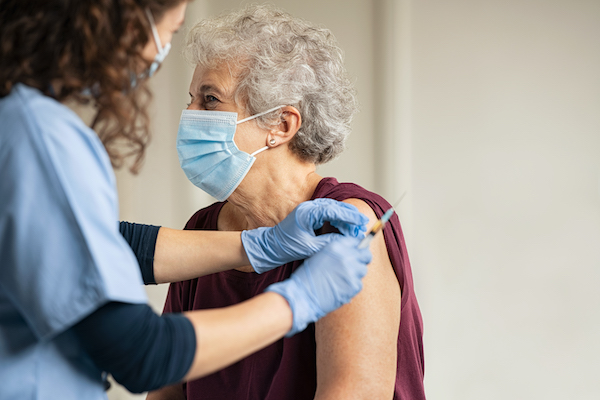
Durabilidad de la eficacia de la vacuna contra el virus sincicial respiratorio
27 noviembre 2025
El estudio reveló que la vacunación contra el VSR fue eficaz para prevenir la enfermedad y el uso de atención médica asociado, pero que la protección disminuyó a lo largo de dos temporadas. Las reducciones fueron más notables en personas inmunodeprimidas, lo que sugiere la necesidad de analizar si dosis adicionales de la vacuna podrían beneficiar a ciertos grupos de riesgo. JAMA Internal Medicine, 25 de noviembre de 2025.

Eficacia de nirsevimab contra la hospitalización por bronquiolitis por VSR en una temporada de alta circulación de VSR-B
11 septiembre 2025
A pesar de la alta circulación del VSR-B en Francia, que recientemente se ha identificado como portador de mutaciones que podrían inducir resistencia al nirsevimab, la eficacia de la segunda campaña nacional de nirsevimab contra la hospitalización por bronquiolitis por VSR se mantuvo alta. The Lancet Regional Health Europe, 10 de septiembre de 2025.
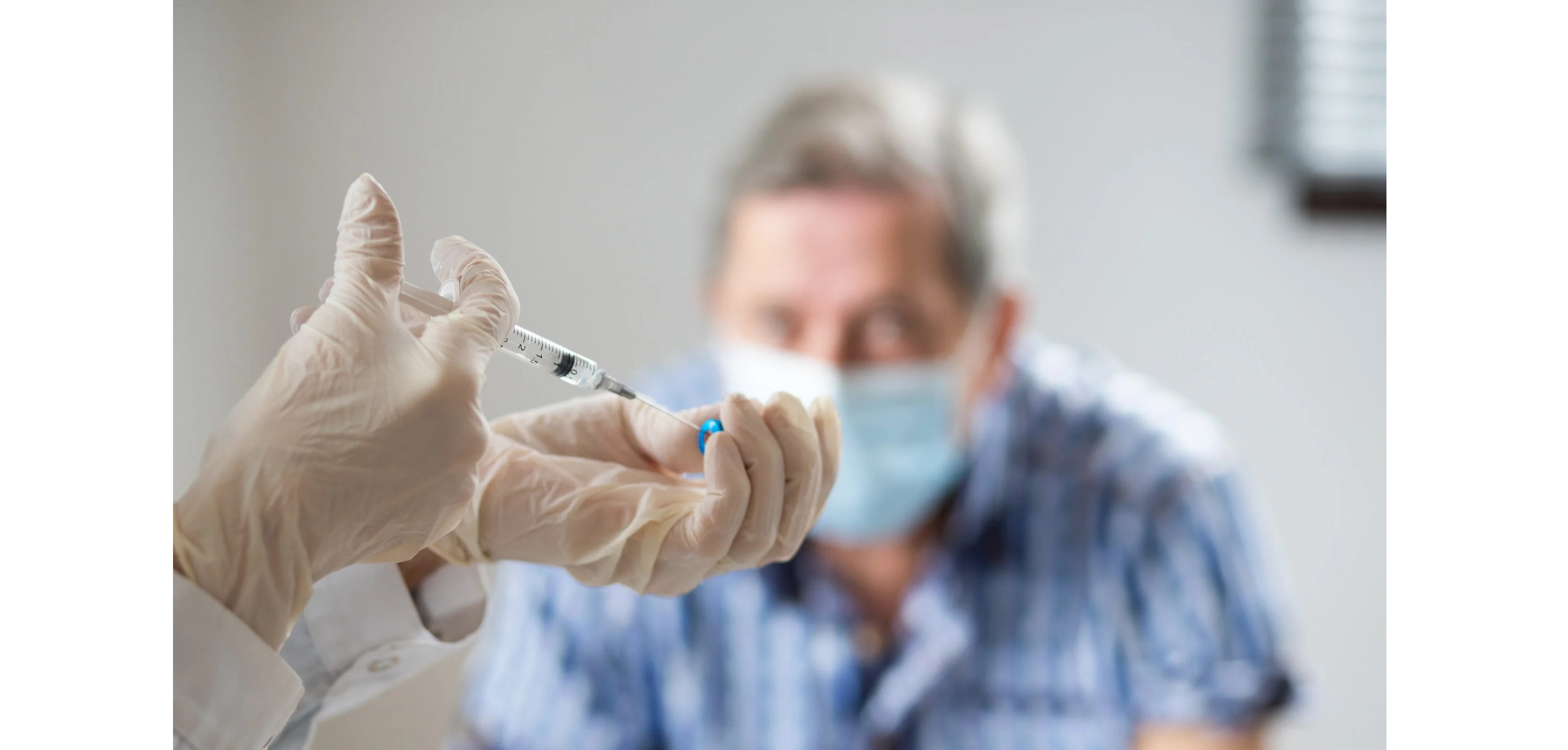
Vacuna anti-VSR Prefusion F para evitar internaciones en adultos mayores
01 septiembre 2025
