Farmacología
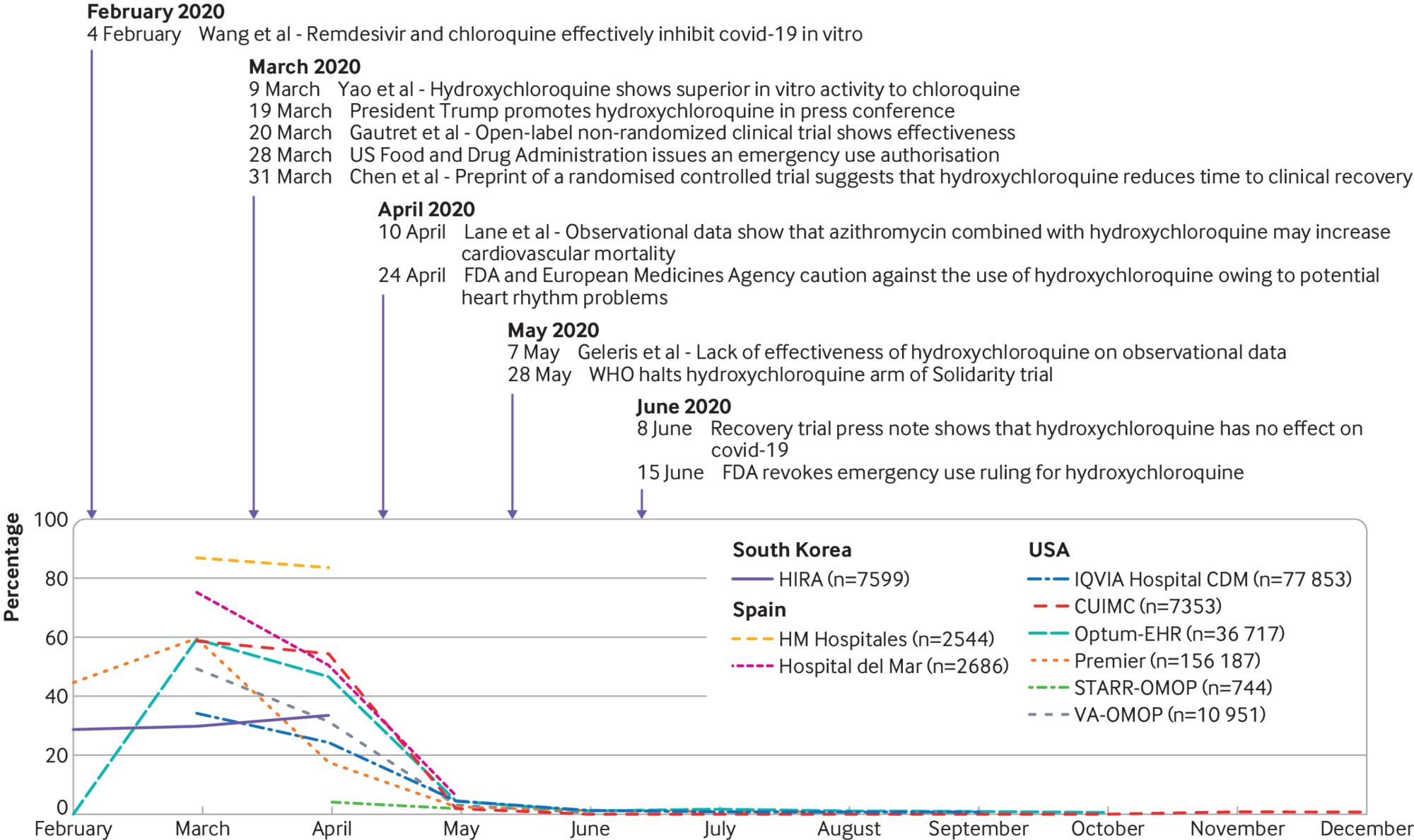
Uso de fármacos adyuvantes y reutilizados en pacientes hospitalarios con covid-19: estudio de cohorte en red multinacional
12 mayo 2021
Se utilizaron múltiples fármacos en los primeros meses de la pandemia de covid-19, con variaciones geográficas y temporales sustanciales. La hidroxicloroquina, azitromicina, lopinavir-ritonavir y umifenovir (solo en China) fueron los fármacos reutilizados más recetados. Los antitrombóticos, antibióticos, antagonistas de los receptores H2 y corticosteroides se utilizaron a menudo como tratamientos complementarios. Se necesita investigación sobre el riesgo comparativo y el beneficio de estos tratamientos en el manejo del covid-19. BMJ 11 de mayo de 2021
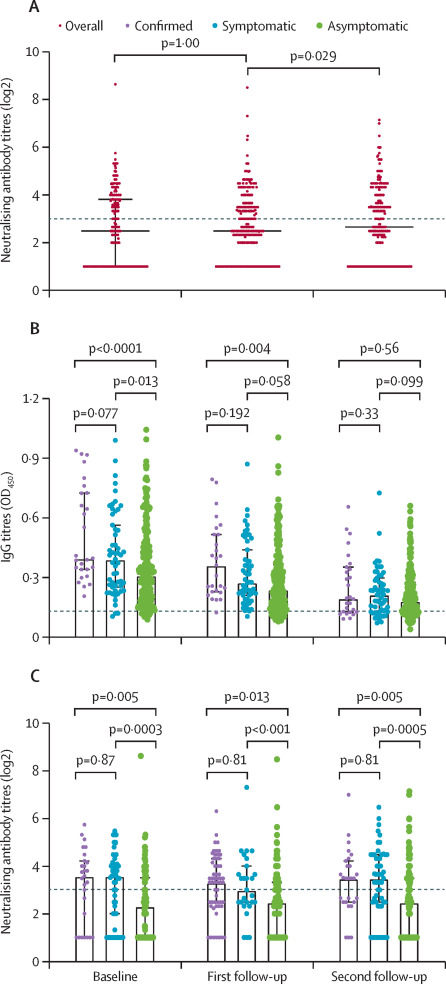
Seroprevalencia y durabilidad inmune humoral de los anticuerpos anti-SARS-CoV-2 en Wuhan, Chin
23 marzo 2021
El 6,92% de una muestra transversal de la población de Wuhan desarrolló anticuerpos contra el SARS-CoV-2, y el 39,8% de esta población seroconvirtió para mantener anticuerpos neutralizantes. Los datos de duración de las respuestas humorales indican que es necesaria la vacunación masiva para alcanzar la protección de rebaño y prevenir el resurgimiento de la epidemia.Lancet, 20 de marzo de 2021
Seguridad, tolerabilidad e inmunogenicidad de una vacuna inactivada (CoronaVac ) contra el SARS-CoV-2 en adultos sanos de 18 a 59 años: ensayo clínico de fase 1/2 aleatorizado, doble ciego, controlado con placebo
18 noviembre 2020
Entre el 16 y el 25 de abril de 2020, se inscribieron 144 participantes en el ensayo de fase 1, y entre el 3 y el 5 de mayo de 2020, se inscribieron 600 participantes en el ensayo de fase 2. Teniendo en cuenta la seguridad, la inmunogenicidad y la capacidad de producción, la dosis de 3 μg de CoronaVac es la dosis sugerida para la evaluación de la eficacia en futuros ensayos de fase 3. Lancet Infect Dis. 17 de noviembre de 2020
Inmunogenicidad y seguridad de una vacuna COVID-19 vectorizada con adenovirus recombinante tipo 5 (Ad5) en adultos sanos de 18 años de edad o mayores: un ensayo aleatorizado, doble ciego, controlado con placebo, fase 2
21 julio 2020
La evidencia de este estudio de fase 2 indica que la vacuna COVID-19 vectorizada con Ad5 candidata tiene un buen perfil de seguridad, con solo eventos adversos leves y transitorios relacionados con la vacunación y sin eventos adversos graves. La inmunización de dosis única con la vacuna indujo un inicio rápido de respuestas inmunes en 14 días y respuestas inmunes humorales y celulares significativas en 28 días en la mayoría de los receptores. Lancet 20 de julio de 2020
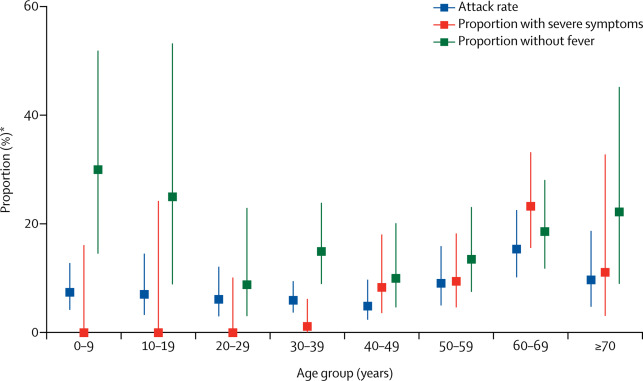
COVID-19: Beneficios detallados del rastreo de contactos en China
29 abril 2020
