Farmacología

Nirmatrelvir-ritonavir oral como profilaxis postexposición para Covid-19
18 julio 2024
En este ensayo controlado con placebo, la profilaxis postexposición con nirmatrelvir-ritonavir durante 5 o 10 días no redujo significativamente el riesgo de infección sintomática por SARS-CoV-2. New England Journal of Medicine, 17 de julio de 2024

Nirmatrelvir y ritonavir (Paxlovid) en Columbia Británica (Canadá): análisis provisional del mundo real
14 febrero 2023
Therapeutics Letter #141 muestra que es posible saber después de que se comercializan nuevos medicamentos si están haciendo más bien que mal con el tiempo. Therapeutics Letters [141], 13 de febrero de 2023

Efectividad de nirmatrelvir más ritonavir en una población ambulatoria vacunada
26 diciembre 2022
Este estudio observacional analizó 44.000 adultos ambulatorios con Covid durante el predominio de la variante omicrón, más del 90% de los cuales habían recibido 3 o más dosis de vacunas para SARS-CoV-2. La tasa de internación o muerte a los 28 días en el grupo control fue de 0.97%, un valor mucho menor que el 7% observado en el grupo placebo en el estudio pivotal de nirmatrelvir; de todos modos, se redujo aún más con el agregado de nirmatrelvir/ritonavir, hasta 0.55%. A medida que varía el estado inmunitario de la población y la virulencia de las cepas predominantes, el efecto absoluto del beneficio de los tratamientos antivirales también se modifica. Annals of Internal Medicine, 13 de diciembre de 2022.
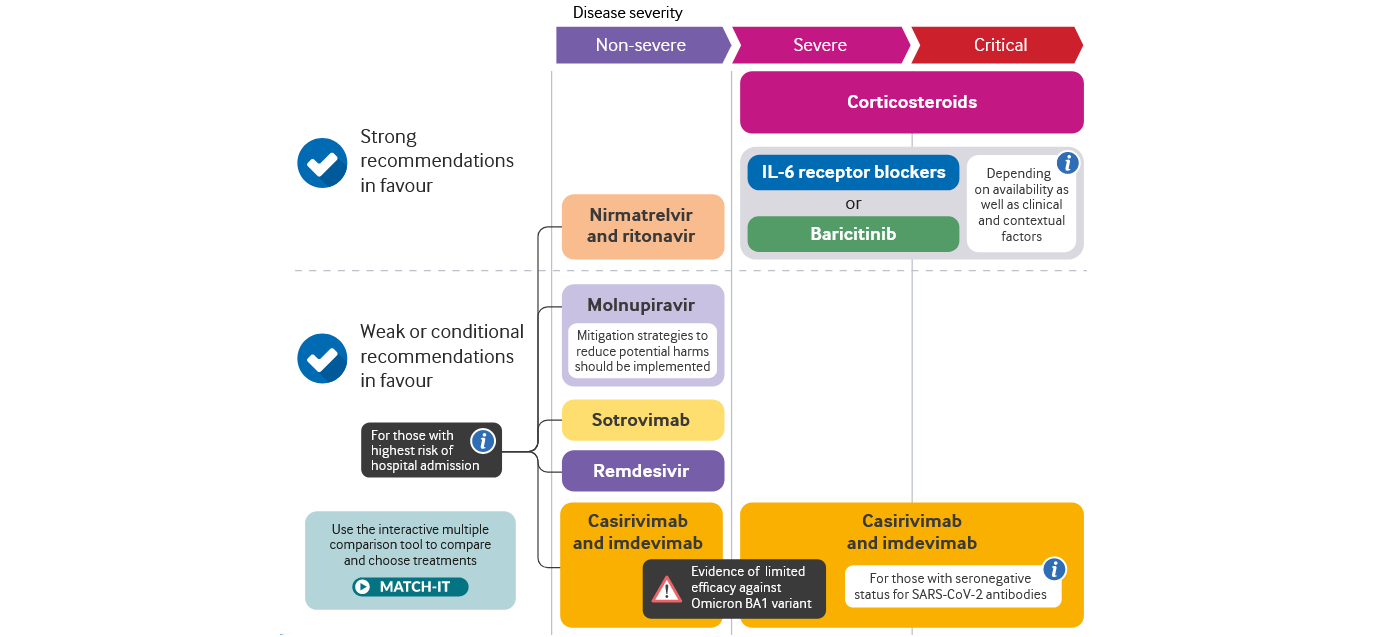
Actualización de la guía de la OMS sobre medicamentos para covid-19
25 abril 2022
En su novena actualización de las guías, la OMS aborda el uso de nirmatrelvir/ritonavir y de remdesivir en pacients con covid-19 no grave, a partir del resultado de nuevos ensayos clínicos. También se ha revisado la estructura de la guía para dar cabida a un número cada vez mayor de opciones de tratamiento eficaces. British Medical Journal, 22 de abril de 2022.

FDA autoriza el primer tratamiento antiviral oral contra el COVID-19: Paxlovid (nirmatrelvir + ritonavir)
23 diciembre 2021
