Farmacología

Seguridad de medicamentos: señales y alertas generadas en 2016
28 junio 2017
INFAC Volumen 25 •nº 04 •2017 CEVIME, junio de 2017 Cuando un medicamento nuevo obtiene la autorización de comercialización, los datos disponibles han permitido a las agencias reguladoras correspondientes asumir que los beneficios del medicamento son superiores a los riesgos, en las condiciones en que se ha estudiado. Por eso son tan importantes los estudios de postcomercialización y el sistema de farmacovigilancia
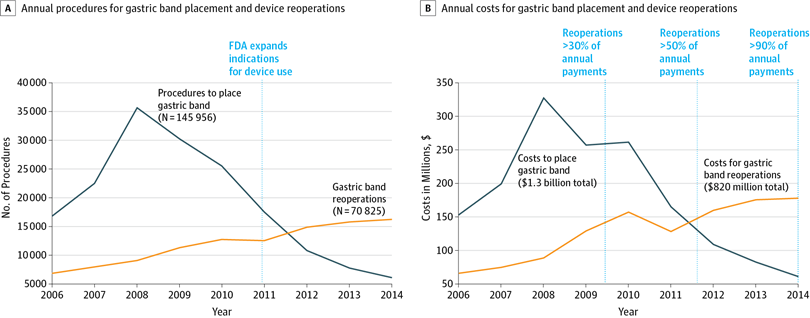
Monitorización de dispositivos médicos. Señales de advertencia perdidas dentro de los datos existentes
28 junio 2017
JAMA, 24 de junio de 2017 Los signos de alerta de atención insegura o de bajo valor son detectables dentro de los datos existentes, pero a menudo se pasan por alto. En lugar de duplicar esfuerzos y recopilar más datos, los líderes de atención de la salud deben renovar su enfoque en hacer un mejor uso de los datos disponibles. Un ejemplo en el que esto es fácilmente evidente implica la monitorización de dispositivos médicos.

Boletín mensual de la AEMPS sobre medicamentos de uso humano del mes de mayo de 2017
27 junio 2017
AEMPS, 19 de junio de 2017

Drug Safety Update Junio 2017
26 junio 2017

