Farmacología
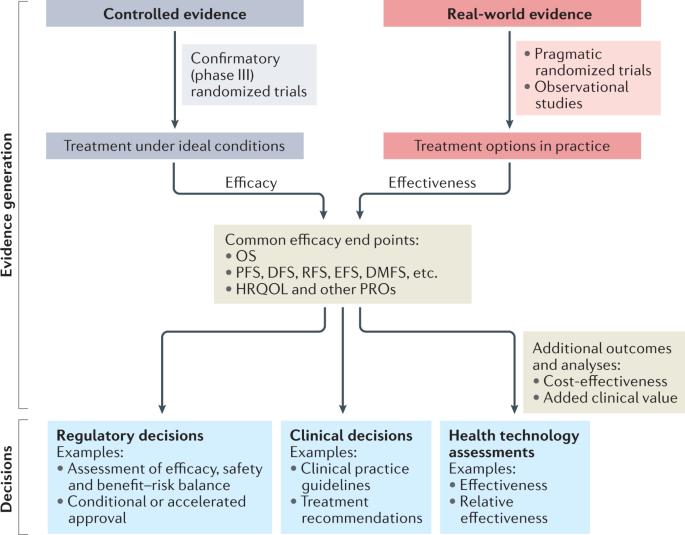
El valor de los medicamentos contra el cáncer: una visión regulatoria
20 abril 2022
Aunque es poco probable que surja una definición única que capte completamente el concepto de valor, aquí discutimos la importancia de comprender las diferentes perspectivas y cómo los reguladores pueden ayudar a informar a los diferentes tomadores de decisiones. Nat Rev Clin Oncol, marzo 2022

Sobre la investigación, desarrollo y producción pública de nuevos medicamentos
05 junio 2020
En este trabajo se discute la problemática de la escasa innovación y cómo, dejar en manos de la industria farmacéutica privada las últimas etapas de investigación y desarrollo de nuevos medicamentos y su producción, ha permitido que las empresas involucradas prioricen sus beneficios económicos y la rentabilidad de sus accionistas, relegando la investigación y desarrollo en nuevos tratamientos que puedan resolver problemas de Salud Pública. Ciencia, tecnología Y política 31 de mayo de 2020

Precios justos: 5) Se necesitan nuevos "modelos de negocio" para la I+D que favorezcan la accesibilidad
17 enero 2020
British Medical Journal, 13 de enero de 2020

Uso de la metodología GRADE para evaluar la innovación de nuevos medicamentos en Italia.
10 diciembre 2019
Los nuevos criterios de innovación de AIFA dieron como resultado un modelo mucho más flexible y transparente para definir y evaluar lo que constituye una innovación terapéutica. En particular, la elección de AIFA para utilizar la metodología GRADE para evaluar la calidad de la evidencia clínica dentro de un proceso de evaluación de la innovación de los medicamentos es esencial para la identificación temprana de la discrepancia entre la necesidad de los pacientes de un acceso rápido a las terapias innovadoras y la disponibilidad Datos clínicos necesarios para tomar decisiones sobre la innovación de los medicamentos. Br J Clin Pharmacol, 7 de octubre de 2019

Valor terapéutico añadido de los nuevos medicamentos aprobados en Brasil desde 2004 a 2016
16 julio 2019
