Farmacología
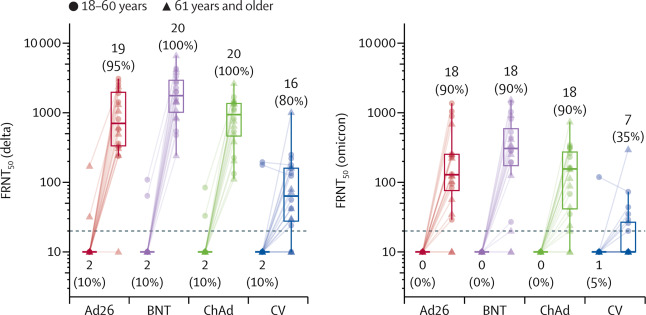
Vacunación de refuerzo de COVID-19 heteróloga versus homóloga en receptores anteriores de dos dosis de la vacuna CoronaVac COVID-19 en Brasil (RHH-001)
24 enero 2022
En este estudio aleatorizado de fase 4, de no inferioridad, simple ciego, las concentraciones de anticuerpos fueron bajas a los 6 meses después de la inmunización previa con dos dosis de CoronaVac. Sin embargo, las cuatro vacunas administradas como una tercera dosis indujeron un aumento significativo en los anticuerpos de unión y neutralización, lo que podría mejorar la protección contra la infección. El refuerzo heterólogo dio como resultado respuestas inmunitarias más robustas que el refuerzo homólogo y podría mejorar la protección. Lancet, 21 de enero de 2022

Parálisis de Bell luego de vacunación con CoronaVac y BNT162b2
17 agosto 2021
Los hallazgos observacionales sugieren un aumento del riesgo de parálisis de Bell después de la vacuna con virus inactivado CoronaVac y un aumento menor, que no alcanzó significación estadística, con la vacuna de ARNm de Pfizer. Sin embargo, los efectos beneficiosos y protectores de las vacunas superan con creces el riesgo de este evento adverso generalmente autolimitado. Se necesitan estudios adicionales para confirmar estos resultados. The Lancet Infectious Diseases, 16 de agosto de 2021.
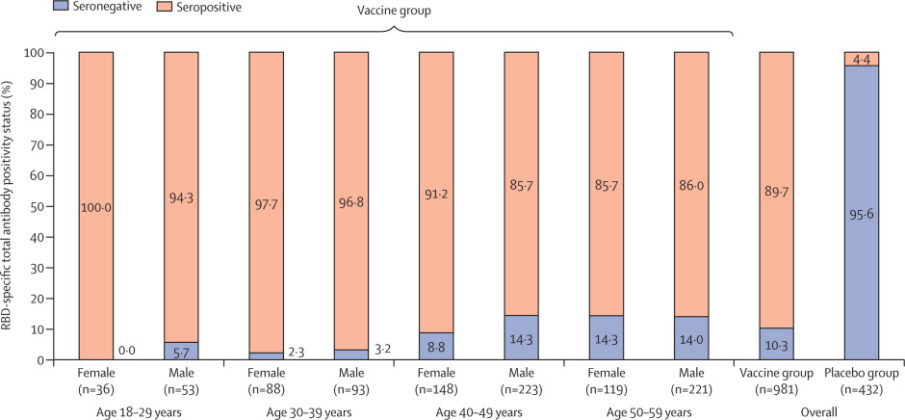
Eficacia y seguridad de una vacuna SARS-CoV-2 de virión completo inactivado (CoronaVac)
13 julio 2021
CoronaVac tiene una alta eficacia contra COVID-19 sintomático confirmado por PCR con un buen perfil de seguridad y tolerabilidad. Lancet, 8 de julio de 2021 “
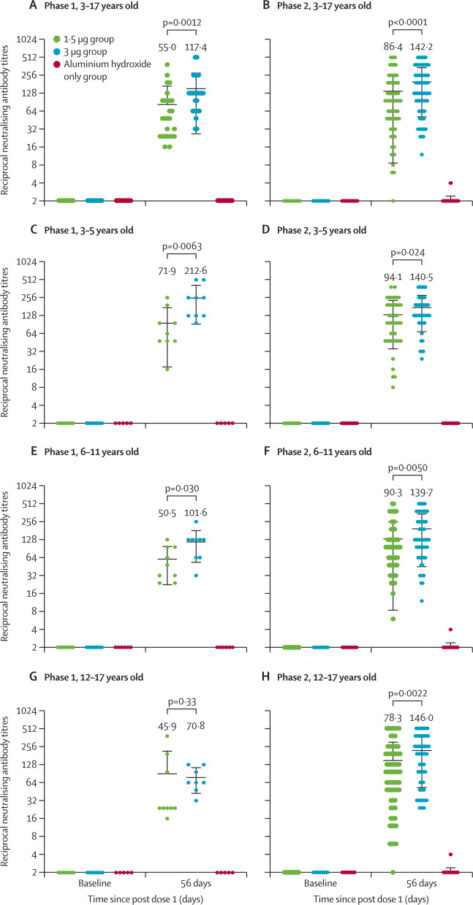
Seguridad, tolerabilidad e inmunogenicidad de la vacuna inactivada contra el SARS-CoV-2 (CoronaVac) en niños y adolescentes
30 junio 2021
CoronaVac es bien tolerada y segura e induce respuestas humorales en niños y adolescentes de 3 a 17 años. Los títulos de anticuerpos neutralizantes inducidos por la dosis de 3,0 µg fueron más altos que los de la dosis de 1,5 µg. Los resultados apoyan el uso de una dosis de 3,0 μg con un calendario de dos inmunizaciones para estudios adicionales en niños y adolescentes. Lancet Infect Dis. 28 de junio de 2021
Seguridad, tolerabilidad e inmunogenicidad de una vacuna inactivada (CoronaVac ) contra el SARS-CoV-2 en adultos sanos de 18 a 59 años: ensayo clínico de fase 1/2 aleatorizado, doble ciego, controlado con placebo
18 noviembre 2020
