Farmacología

Aumento de sobredosis y muertes relacionadas con la metadona durante la epidemia de COVID-19 en 2020
03 julio 2023
Los datos de este trabajo muestran un aumento de la morbilidad y la mortalidad relacionadas con la metadona durante la epidemia de COVID-19. Esta tendencia se ha observado en otros países. Therapie, 15 de junio de 2023
Reacciones adversas a medicamentos utilizados para la COVID-19 en cinco países de América Latina
03 octubre 2022
Si bien no es posible establecer una relación causal a partir de la evaluación de informes espontáneos, el presente estudio confirma la presencia de reacciones adversas, algunas graves, con medicamentos que se utilizaron para tratar o prevenir la COVID-19. Rev Panam Salud Publica, 27 de septiembre de 2022

Seguridad de medicamentos y sustancias de uso frecuente para automedicación en COVID-19
04 mayo 2022
El objetivo de esta revisión es describir la evidencia disponible sobre la eficacia, seguridad y seguimiento de los fármacos y sustancias que han demostrado ser de uso frecuente para la automedicación en pacientes con COVID-19 (hidroxicloroquina, antiinflamatorios no esteroideos, antiinflamatorios, ivermectina, azitromicina, vitaminas, aspirina y dióxido de cloro) para caracterizar adecuadamente sus riesgos, uso seguro, estrategias de vigilancia y reforzar el concepto de que estas sustancias no deben utilizarse para la automedicación y requieren prescripción médica. Ther Adv Drug Saf, 21 de abril de 2022

CDC: Seguridad de la vacuna BNT162b2 (Pfizer-BioNTech) contra la COVID-19 en niños de 5 a 11 años, luego de 8,7 millones de dosis, en Estados Unidos
21 enero 2022
Después de la autorización de la vacuna Pfizer-BioNTech COVID-19 para niños de 5 a 11 años durante octubre de 2021, y la administración de aproximadamente 8 millones de dosis, las reacciones locales y sistémicas después de la vacunación se informaron comúnmente a VAERS y v-safe para niños vacunados de 5 a 11 años. Rara vez se informaron eventos adversos graves. Se debe informar a los padres y tutores de niños de 5 a 11 años que se esperan reacciones locales y sistémicas después de la vacunación con la vacuna Pfizer-BioNTech COVID-19 y que son más comunes después de la segunda dosis. MMWR Morb Mortal Wkly Rep, 31 de diciembre de 2021
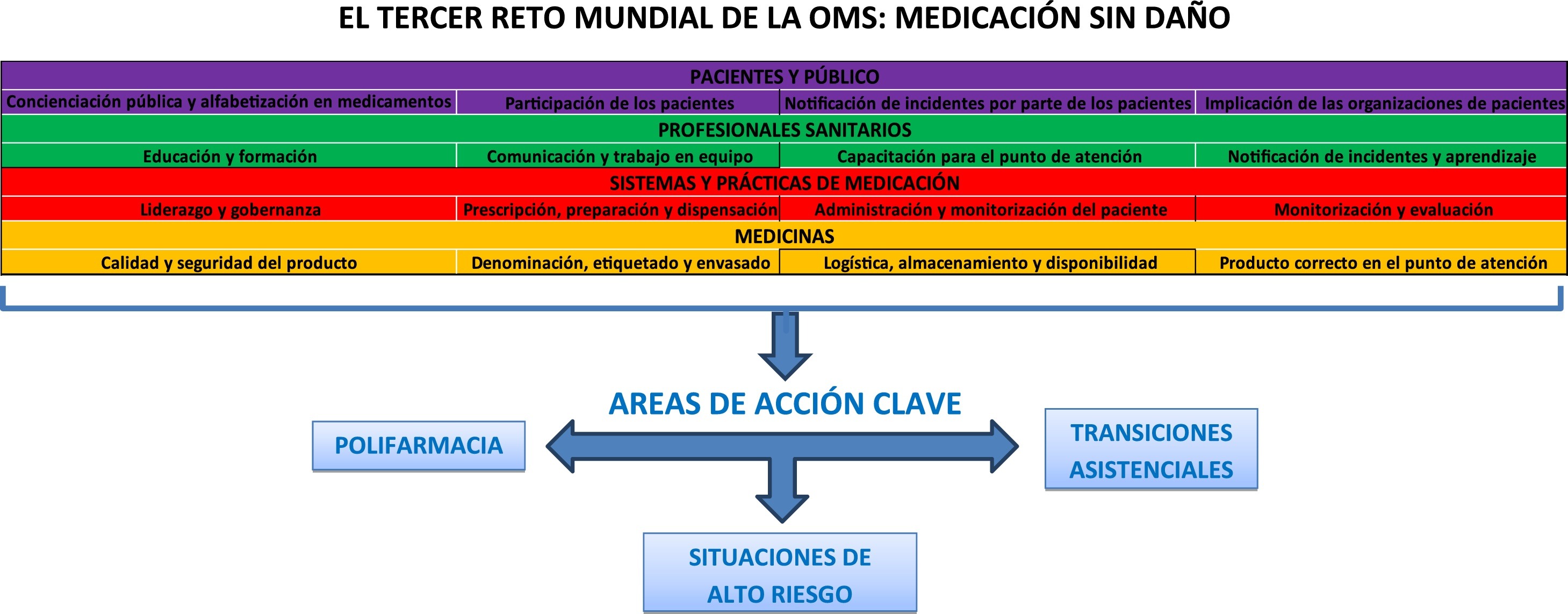
Uso seguro de los medicamentos en Atención Primaria, también en época de pandemia de la COVID-19
27 diciembre 2021
