Farmacología

Datos del mundo real y evidencia del mundo real en la toma de decisiones regulatorias: Resumen del informe del Grupo de trabajo XIII del Consejo de Organizaciones Internacionales de Ciencias Médicas (CIOMS)
28 abril 2025
Un informe reciente de un grupo de trabajo del Consejo de Organizaciones Internacionales de las Ciencias Médicas (CIOMS) describe el uso de la evidencia del mundo real (RWE) para la toma de decisiones en el ciclo de vida de los productos médicos, describe los datos del mundo real (RWD) y las fuentes de datos, analiza las consideraciones científicas clave en la generación de la RWE y aborda los aspectos éticos y de gobernanza relacionados con su uso. Pharmacoepidemiol Drug Saf. marzo de 2025

La ANMAT autorizó la comercialización de mifepristona
08 marzo 2023
Esta disposición completa el paquete regulatorio básico necesario para asegurar la disponibilidad de los mejores estándares de atención y clínicos en todos los efectores de salud del país para la atención integral de las personas con derecho a la interrupción voluntaria y legal del embarazo. Ministerio de Salud de la Nación, 8 de Marzo de 2023
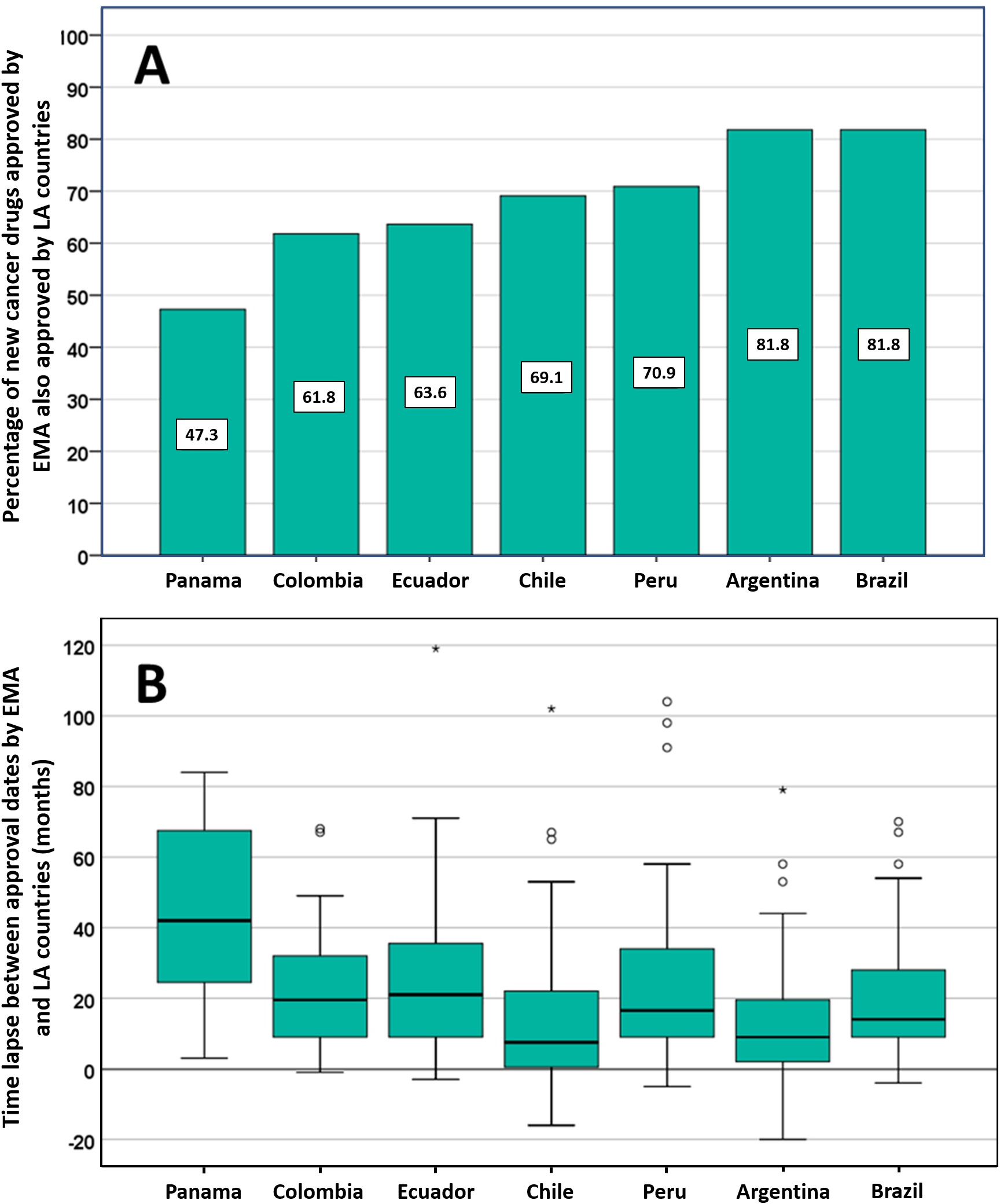
Posible impacto negativo de las decisiones de Agencias reguladoras reputadas sobre el estado de aprobación de nuevos medicamentos contra el cáncer en los países de América Latina
14 julio 2021
Los países de América Latina siguen aprobando nuevos medicamentos contra el cáncer, a menudo basándose en ensayos clínicos mal realizados que miden criterios de valoración sustitutos. La EMA y otros reguladores de renombre deben ser conscientes de que sus decisiones regulatorias pueden influir directamente en las decisiones relativas a la autorización de comercialización, los presupuestos de salud y la atención del paciente en otros lugares. PLoS ONE 13 de julio de 2021
Asociación entre los programas de aprobación acelerada de la FDA y la EMA y el valor terapéutico de los nuevos medicamentos: estudio de cohorte retrospectivo
08 octubre 2020
Menos de un tercio de los nuevos medicamentos aprobados por la FDA y la EMA durante la última década fueron calificados como de alto valor terapéutico por al menos una de las cinco organizaciones independientes. Aunque los medicamentos acelerados tenían más probabilidades de tener una calificación alta que los medicamentos no acelerados, la mayoría de los medicamentos acelerados aprobados por la FDA, pero no por la EMA, fueron calificados como de bajo valor terapéutico. BMJ 7 de octubre de 2020

Aprobación y regulación de productos farmacéuticos de la FDA, 1983-2018
15 enero 2020
