Farmacología

Más allá de la etiqueta: Replanteando el uso de medicamentos fuera de indicación en pediatría. Hacia un futuro con base científica y más seguro para la farmacoterapia pediátrica.
18 febrero 2026
Esta revisión narrativa examina las estrategias para mitigar los riesgos asociados con el uso de medicamentos no aprobados en pediatría y propone un marco de cinco pasos .Cerrar las brechas de conocimiento mediante la priorización de la investigación, el mapeo de la evidencia y metodologías innovadoras como la extrapolación, el modelado y la simulación pediátricos, el uso de evidencia real y diseños de ensayos innovadores permitirá un uso fuera de indicación más seguro y con base científica. La difusión a través de plataformas internacionales armonizadas de información sobre medicamentos pediátricos es fundamental para garantizar el acceso equitativo a la farmacoterapia pediátrica con la mejor evidencia científica. Br J Clin Pharmacol, 15 de febrero de 2026

Tendencias, variación geográfica y factores asociados con la prescripción de melatonina en la práctica general en Inglaterra
12 noviembre 2021
La prescripción de melatonina en Inglaterra ha aumentado exponencialmente durante la última década, con un gasto sustancial en productos sin licencia de calidad desconocida. Se necesita investigación de análisis a nivel de paciente. Br J Clin Pharmacol , 7 de noviembre de 2021

Recetas de medicamentos por fuera de los usos aprobados (off label) en la práctica general francesa: un estudio transversal
11 abril 2019
BMJ Open, 9 de abril de 2019 Casi un 20% de los fármacos fueron prescriptos por fuera de los usos aprobados

Coordinando el cumplimiento de reealización de ensayos clínicos para confirmar la seguridad y eficacia de los medicamentos: resolución de incertidumbres
10 enero 2019
JAMA Intern Med. 4 de enero de 2019 ¿Cómo sabemos si un medicamento funciona? En los Estados Unidos, la Administración de Medicamentos y Alimentos de los Estados Unidos (FDA, por sus siglas en inglés) ha establecido una guía para informar el desarrollo de medicamentos, incluidas las pruebas para establecer la seguridad y eficacia de una indicación clínica específica, antes de la aprobación del mercado. Sin embargo, una vez aprobado, los médicos pueden recetar el medicamento para cualquier indicación clínica, no solo la que recibió la aprobación de la FDA. Esto se conoce como prescripción off-label.
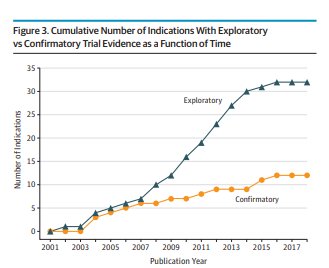
Evaluación de los ensayos postaprobación de pregabalina y sugerencia de eficacia para nuevas indicaciones: revisión sistemática
09 enero 2019
