Farmacología
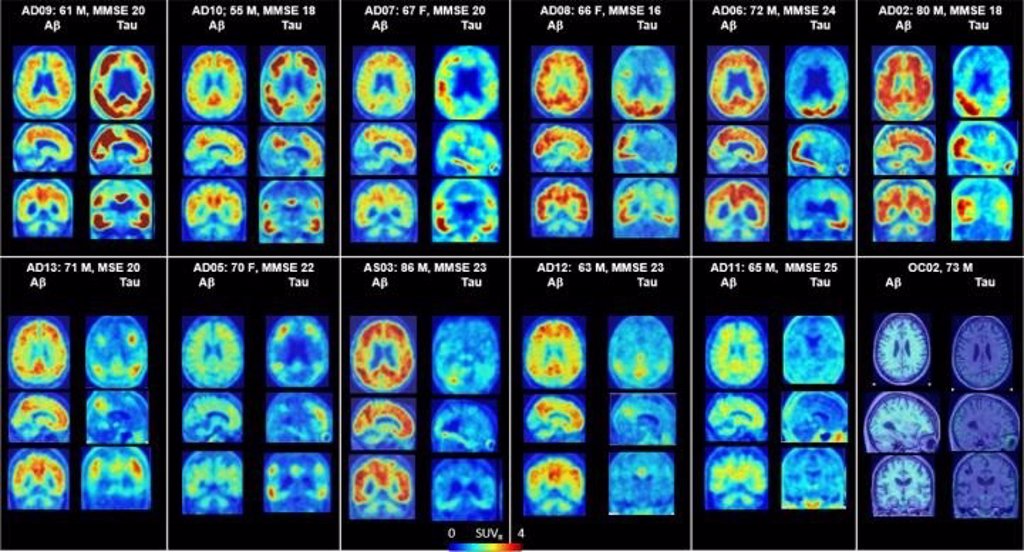
Desafíos con nuevos tratamientos para la enfermedad de Alzheimer. La aprobación acelerada de aducanumab en los Estados Unidos plantea interrogantes
14 abril 2023
Los médicos de familia suelen ser los primeros médicos en evaluar a las personas con síntomas cognitivos de EA y los primeros en recibir preguntas sobre nuevos medicamentos y posibles avances en el tratamiento. Muchos médicos ya han hecho que los pacientes pregunten sobre aducanumab. Aquí proporcionamos una descripción general de este agente y su estado actual. Can Fam Physician. marzo de 2023
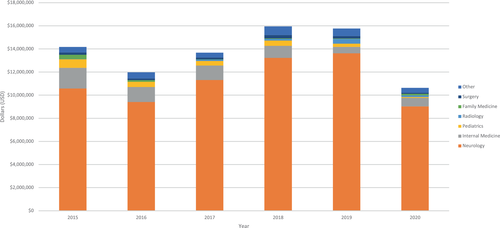
Pagos generales de Biogen a médicos estadounidenses entre 2015 y 2020
13 junio 2022
Los pagos financieros son una estrategia de marketing generalizada utilizada por las compañías farmacéuticas y no se limitan a los médicos, sino a las partes interesadas de la medicina, como academias nacionales,8 editores de revistas, enfermeras practicantes y asistentes médicos. Además, más de dos tercios del Congreso de los EE. UU. recibió pagos de las principales compañías farmacéuticas en 2020, como Pfizer, Amgen, Biogen, entre otras. Esto es preocupante, ya que numerosos estudios han encontrado que los pagos financieros influyen en el comportamiento hacia una mayor prescripción, prescripciones más costosas y un mayor uso de medicamentos de marca. En el caso de aducanumab, los incentivos para aumentar la prescripción exacerbarían los impactos negativos previstos en el sistema de salud y los pacientes en todo el país. J Am Geriatr Soc. 4 de junio de 2022

Aprobación de medicamentos por la FDA y la ética de la desesperación
29 octubre 2021
Cuando los pacientes tienen un diagnóstico de desesperación que los deja frente a una enfermedad que limita la vida sin buenas opciones de tratamiento, ¿qué papel debe desempeñar su voluntad de probar un medicamento de beneficio no probado en la toma de decisiones regulatorias? En este punto de vista, argumentamos que las voces de los pacientes deben integrarse en el proceso de aprobación de medicamentos, pero sin tal deferencia que la FDA abdique de su responsabilidad de garantizar que los medicamentos sean seguros y efectivos. JAMA Intern Med, 25 de octubre de 2021

¿Deberían las autoridades reguladoras aprobar medicamentos basados en desenlaces subrogados?
17 septiembre 2021
La controversia del aducanumab es el último ejemplo de criterios de valoración sustitutos que no predicen resultados clínicamente importantes. Sin embargo, como informan Jeanne Lenzer y Shannon Brownlee, se utilizan cada vez más como la base para las aprobaciones de medicamentos. BMJ 16 de septiembre de 2021

Críticas a la aprobación acelerada por la FDA de un medicamento para el Alzheimer
19 julio 2021
