Farmacología

Preocupación por la falta de competencia en el mercado de los medicamentos
15 septiembre 2020
El American College of Physicians considera que se precisan nuevas políticas para prevenir la manipulación del mercado y ayudar a que las alternativas de menor costo lleguen al mercado más rápido, garantizando un mercado robusto y competitivo para medicamentos genéricos y biosimilares. Annals of Internal Medicine, 15 de septiembre de 2020.
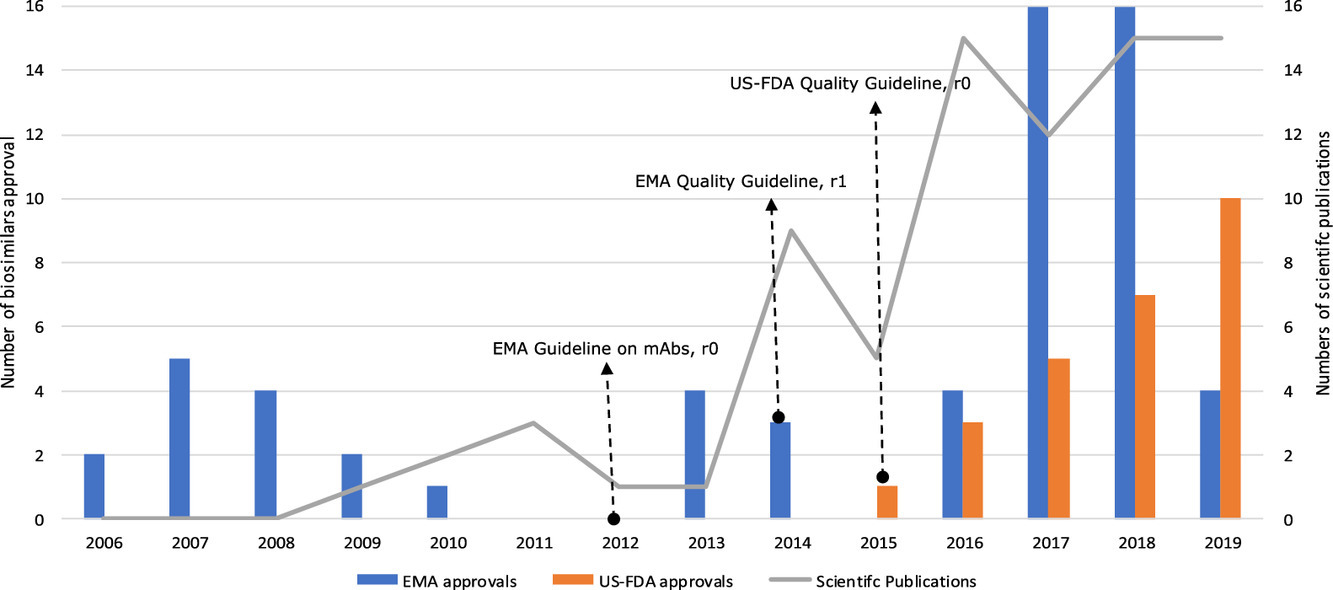
Informe de atributos de calidad en publicaciones científicas que presentan evaluaciones de biosimilaridad de biosimilares (previstos): una revisión sistemática de la literatura
31 julio 2020
Las evaluaciones de biosimilaridad de los atributos de calidad (QA) se han publicado en publicaciones científicas revisadas por pares para aproximadamente el 60% de los biosimilares aprobados. La dinámica de las publicaciones y los tipos de QA de informes aumentaron con el tiempo en paralelo con un mayor número de biosimilares con licencia y parece verse afectada por el desarrollo de pautas regulatorias en 2012-2015.La disponibilidad de una evaluación completa, públicamente accesible (acceso abierto) e imparcial de biosimilaridad de QA podría contribuir a una mayor confianza y aceptación de biosimilares en la práctica clínica. Eur J Pharm Sci, 30 de julio de 2020

Precios justos: 3) Estrategias para lograr precios más justos para medicamentos genéricos y biosimilares
15 enero 2020
Alessandra Ferrario y colegas afirman que la entrada temprana al mercado y la rápida incorporación de genéricos y biosimilares con garantía de calidad son clave para mejorar el acceso a los medicamentos. BMJ 13 de enero de 2020

Evidencia clínica que respalde la autorización de comercialización de biosimilares en Europa
06 enero 2020
El análisis de la aprobación de biosimilares en Europa muestra un escenario complejo y heterogéneo. El requisito de mostrar similitud en términos de eficacia clínica y seguridad proporciona una demostración sólida de resultados clínicos comparables, pero supone una carga para los fabricantes de biosimilares y puede retrasar la introducción de los medicamentos. El desarrollo, la concesión de licencias y la supervisión de los biosimilares se beneficiarían de nuevas estrategias para acelerar el acceso a estos medicamentos y reducir las incertidumbres sobre su uso en la práctica. Eur J Clin Pharmacol , 2 de enero de 2020

Biosimilares: una nueva era en el acceso al tratamiento del cáncer de mama
03 enero 2020
