Farmacología

FDA permite condiciones de almacenamiento y transporte más flexibles para la vacuna Pfizer-BioNTech COVID-19
26 febrero 2021
La actualización proporciona una temperatura alternativa para el transporte y el almacenamiento temporal de los viales congelados antes de la dilución. Permitirá que los viales congelados sin diluir de la vacuna Pfizer-BioNTech COVID-19 se transporten y almacenen a las temperaturas convencionales que se encuentran comúnmente en los congeladores farmacéuticos durante un período de hasta dos semanas FDA, 25 de febrero de 2021
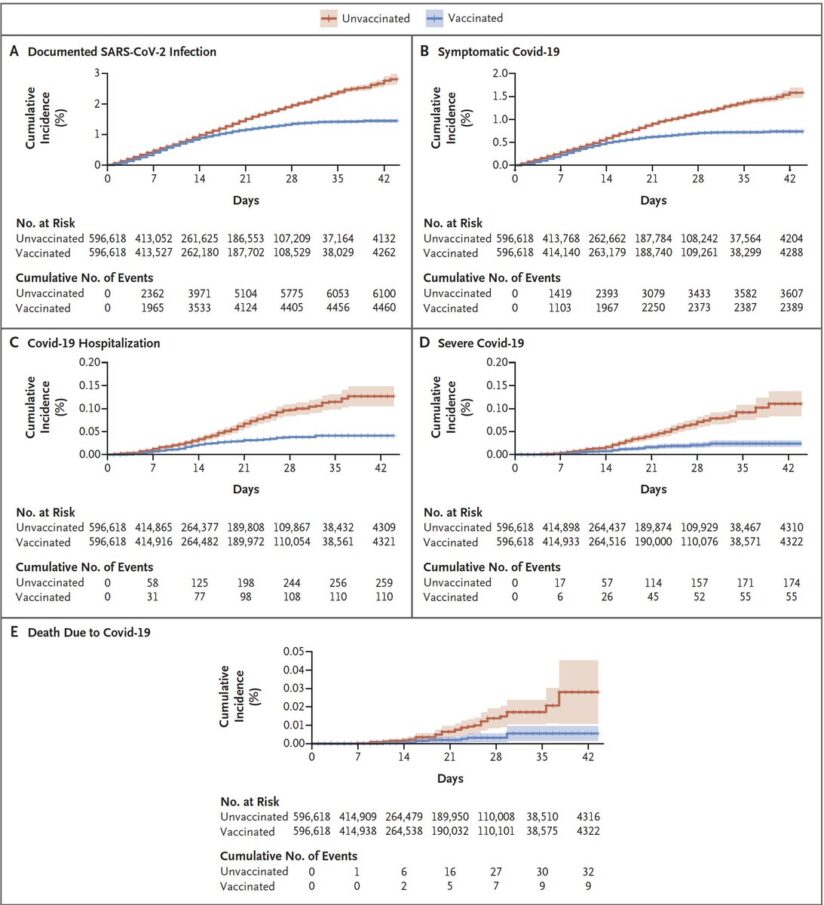
Vacuna Pfizer/BioNTech paraCovid-19 en un entorno de vacunación masiva a nivel nacional
25 febrero 2021
Este estudio en un entorno de vacunación masiva nacional sugiere que la vacuna de ARNm BNT162b2 (tozinameran) es eficaz para una amplia gama de resultados relacionados con Covid-19, un hallazgo consistente con el del ensayo aleatorizado. N Engl J Med, 24 de febrero de 2021

Vacunación COVID-19 en mujeres embarazadas y lactantes
11 febrero 2021
Dado lo que se sabe sobre las vacunas COVID-19, los datos limitados sobre las vacunas COVID-19 en mujeres embarazadas y lactantes de las que han sido inmunizadas, y el uso de otras vacunas durante el embarazo, los médicos pueden empoderar a las mujeres para que tomen una decisión informada. JAMA, 8 de febrero de 2021

España: 2º Informe de Farmacovigilancia sobre Vacunas COVID-19
10 febrero 2021
Hasta el 24 de enero de 2021, se han administrado en España 1.131.805 dosis de vacunas COVID-19 (98% de las dosis administradas correspondieron a Comirnaty y el 2% a la vacuna Moderna), habiéndose recibido 1.555 notificaciones de acontecimientos adversos. Los acontecimientos más frecuentemente notificados siguen siendo los trastornos generales (fiebre, dolor en la zona de inyección), del sistema nervioso central (cefalea, mareos) y del aparato digestivo (náuseas, diarrea). Tras la revisión de los datos disponibles, no se ha identificado ninguna reacción adversa hasta ahora desconocida que pueda ser motivo de preocupación. AEMPS , 9 de febrero de 2021.
Seguridad y eficacia preliminar de las vacunas para la prevención de COVID-19.
27 enero 2021
