Farmacología
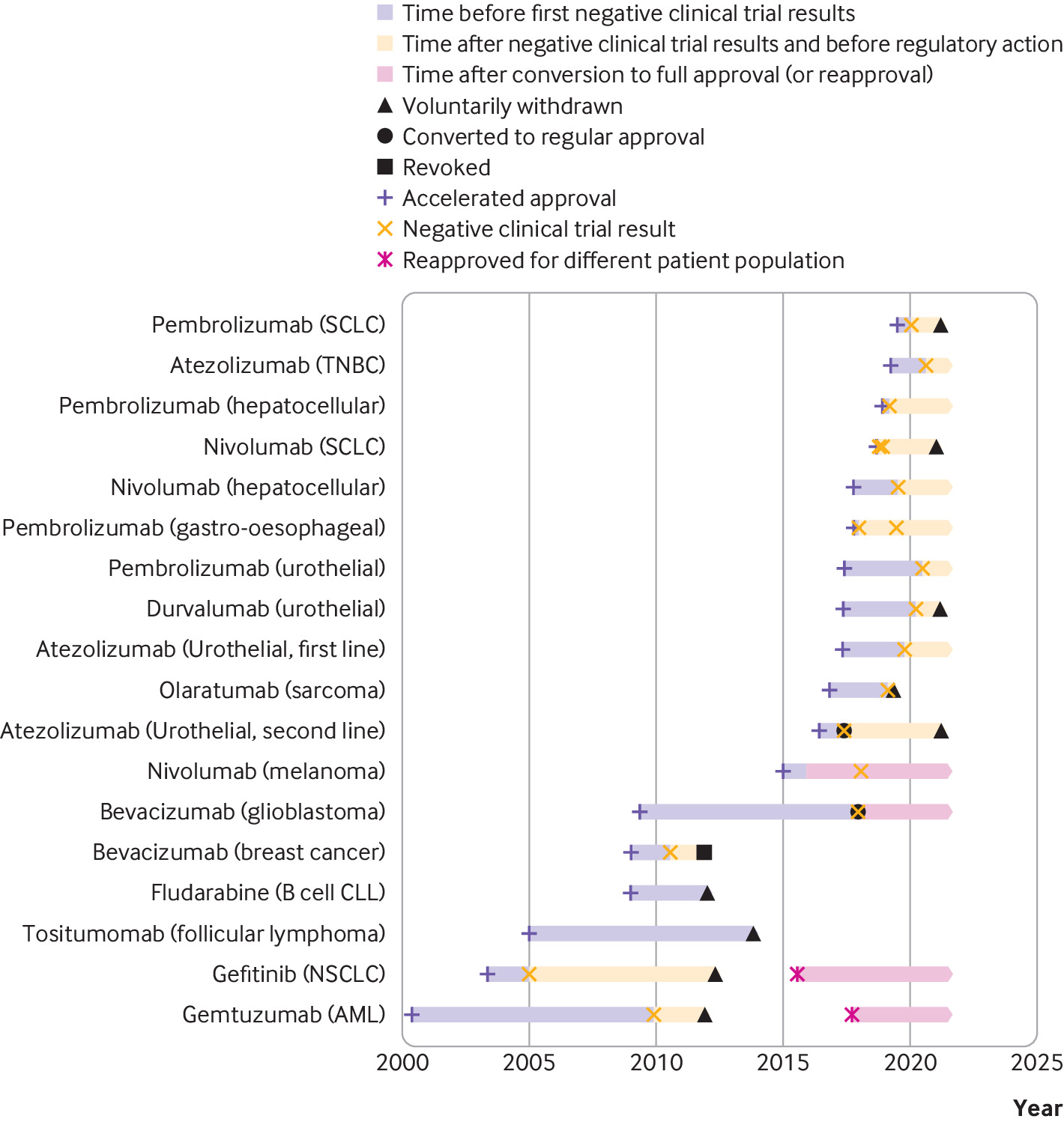
Consecuencias regulatorias y clínicas de los ensayos confirmatorios negativos de medicamentos contra el cáncer de aprobación acelerada
13 septiembre 2021
Las indicaciones de medicamentos contra el cáncer que recibieron una aprobación acelerada a menudo permanecieron en el etiquetado formal de medicamentos aprobados por la FDA y continuaron recomendándose en las guías clínicas varios años después de que los ensayos posteriores a la aprobación requeridos por ley no mostraran una mejoría en el criterio de valoración de eficacia primario. Las guías clínicas deben alinearse mejor con los resultados de los ensayos posteriores a la aprobación de medicamentos contra el cáncer que recibieron una aprobación acelerada. BMJ, 9 de septiembre de 2021

Evaluación de los informes post comercialización con resultado de muerte, en el sistema de notificación de eventos adversos de la FDA de EE. UU.
30 enero 2020
Drug Saf , 24 de enero de 2020 Comprender los orígenes y las características de los informes de seguridad de casos individuales (ICSR) con un resultado de muerte respalda las evaluaciones e interpretaciones significativas de los datos de FAERS. Existe una amplia variabilidad en la calidad de ICSR, incluso en aquellos informes con el resultado más grave.

Registros en la vigilancia postcomercialización europea: un análisis retrospectivo de los productos aprobados por vía centralizada, 2005-2013.
13 julio 2017
Pharmacoepidemiol Drug Saf. 2017 los retrasos en la puesta en marcha de los nuevos registros apoyan la necesidad de mejorar la puntualidad de la recopilación de datos en el contexto posterior a la comercialización

Fármacos para trastornos raros
30 junio 2017
