Farmacología

Evidencias poscomercialización de medicamentos contra el cáncer en la toma de decisiones clínicas y regulatorias: revisión exploratoria
06 febrero 2025
En general, estos hallazgos plantean preguntas importantes en torno a la disponibilidad, accesibilidad y evaluación de la evidencia posterior a la comercialización sobre los beneficios y daños de los medicamentos contra el cáncer, de modo que puedan ser utilizados por los profesionales de la salud que trabajan en servicios oncológicos y por las personas con cáncer. Pharmacoepidemiol Drug Saf. enero de 2025

Seguridad de los medicamentos para enfermedades cardiovasculares aprobados entre 2014 y 2021 en EE. UU.: un análisis de farmacovigilancia
22 mayo 2024
Este estudio identificó preocupaciones de seguridad específicas relacionadas con los medicamentos para enfermedades cardiovasculares aprobados recientemente. Se requiere más investigación para comprender los mecanismos subyacentes y las implicaciones clínicas de estos hallazgos. Expert Rev Cardiovasc Ther. 12 de mayo de 2024

Desacuerdos entre revisores regulatorios de la FDA de EE. UU. para nuevos tratamientos y acciones de seguridad posteriores a la comercialización
23 marzo 2023
Esta investigación de los desacuerdos de los revisores regulatorios y las acciones de seguridad posteriores a la comercialización entre las nuevas terapias sugiere que los desacuerdos entre los revisores regulatorios pueden conducir a importantes acciones preventivas, lo que podría mitigar la necesidad de tomar medidas de seguridad posteriores a la comercialización. BMJ Evidence-Based Medicine, 21 de marzo de 2023
Veinte años de medicamentos inmunomoduladores biológicos y dirigidos: Modificaciones posteriores a la comercialización del etiquetado de los medicamentos aprobados por la FDA
08 agosto 2022
Los problemas de seguridad asociados con los fármacos inmunomoduladores biológicos y dirigidos a menudo se identifican después de la comercialización, con intervalos de tiempo considerables después de la aprobación inicial. Los médicos deben seguir de cerca las actualizaciones de los perfiles de seguridad de los medicamentos inmunomoduladores y estar atentos a los eventos adversos no identificados previamente. Mayo Clin Proc, agosto de 2022
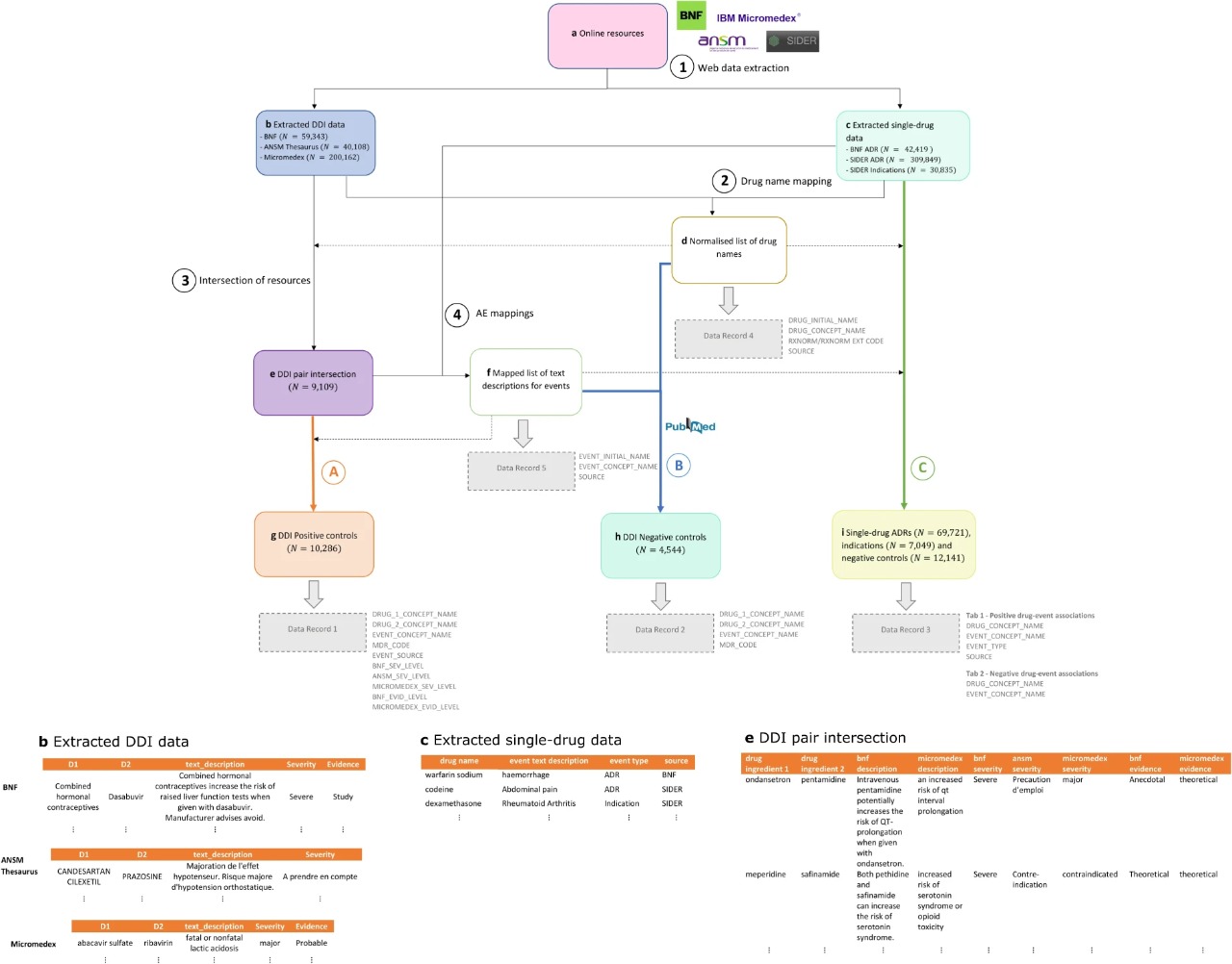
Conjunto de referencia de interacciones farmacológicas adversas clínicamente relevantes
10 marzo 2022
