Farmacología
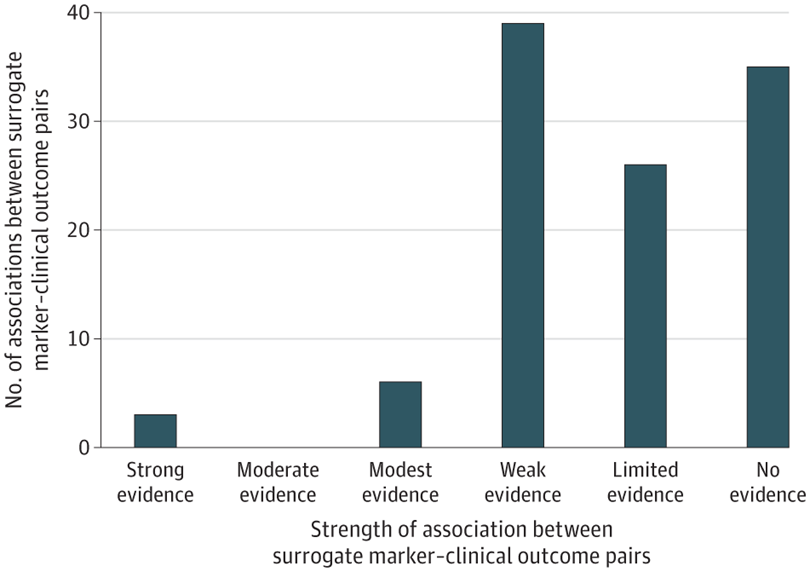
Asociaciones entre marcadores sustitutos y resultados clínicos para tratamientos de enfermedades crónicas no oncológicas
28 mayo 2024
La mayoría de las variables subrogadas utilizadas como puntos finales primarios en ensayos clínicos para respaldar la aprobación de la FDA de medicamentos para el tratamiento de enfermedades crónicas no oncológicas carecían de evidencia sólida de asociaciones con resultados clínicos de los metanálisis publicados. JAMA 22 de abril de 2024

Limitaciones de los desenlaces sustitutos en la aprobación acelerada de nuevos medicamentos
17 septiembre 2021
Aunque los criterios de valoración sustitutos se utilizan ampliamente para acelerar la aprobación de nuevos fármacos, la mayoría no son predictores fiables de los resultados que más importan a los pacientes. Los reguladores sólo deben aceptar criterios de valoración sustitutos cuando no sea posible generar datos sobre los resultados clínicos. British Medical Journal, 16 de septiembre de 2021.
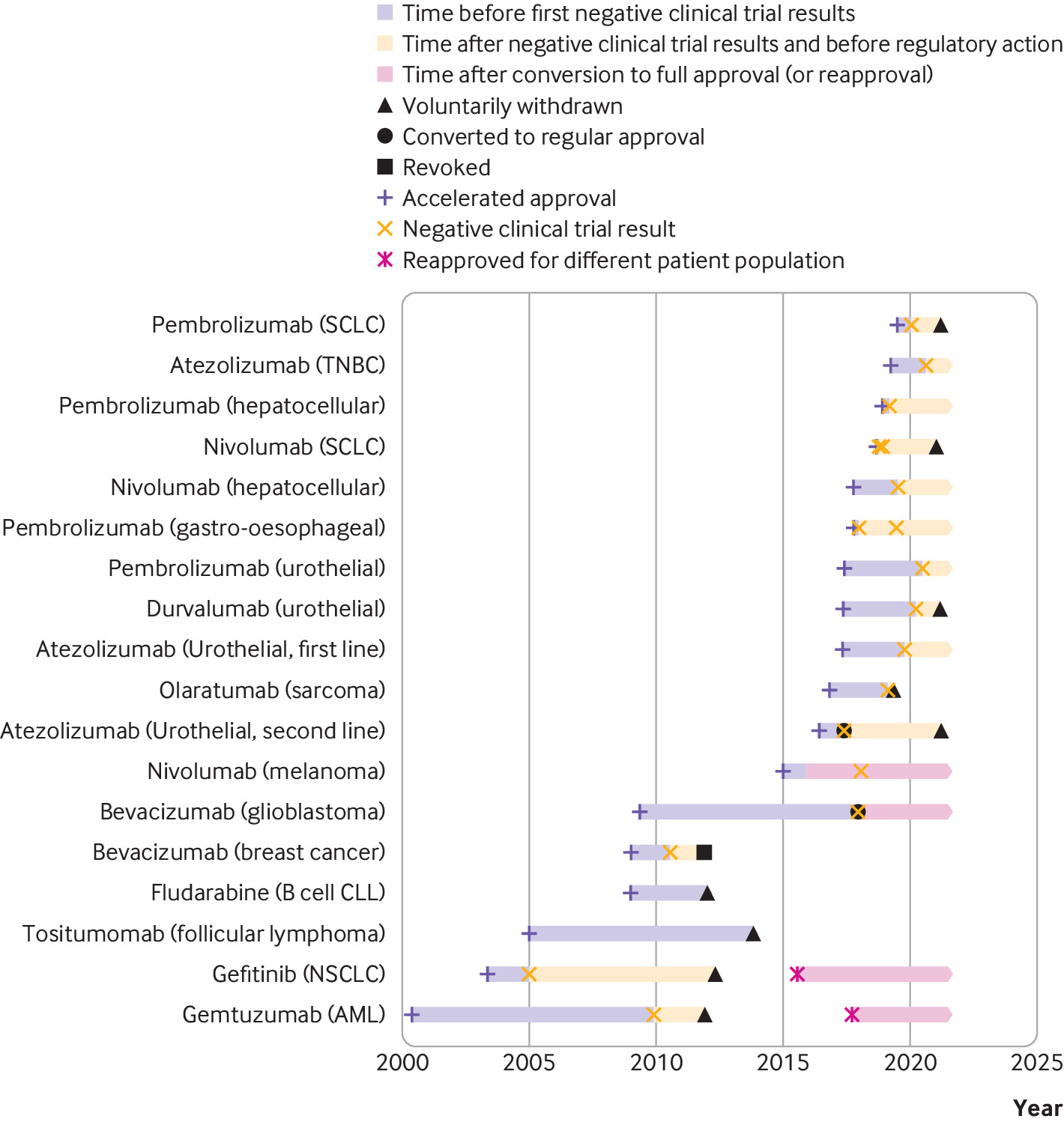
Consecuencias regulatorias y clínicas de los ensayos confirmatorios negativos de medicamentos contra el cáncer de aprobación acelerada
13 septiembre 2021
Las indicaciones de medicamentos contra el cáncer que recibieron una aprobación acelerada a menudo permanecieron en el etiquetado formal de medicamentos aprobados por la FDA y continuaron recomendándose en las guías clínicas varios años después de que los ensayos posteriores a la aprobación requeridos por ley no mostraran una mejoría en el criterio de valoración de eficacia primario. Las guías clínicas deben alinearse mejor con los resultados de los ensayos posteriores a la aprobación de medicamentos contra el cáncer que recibieron una aprobación acelerada. BMJ, 9 de septiembre de 2021

Tamaño de la población de seguridad pre-comercialización asociado con medicamentos del programa de aprobación acelarada y medicamentos huérfanos
23 octubre 2019
Este estudio da cuenta si una gran población de seguridad, definida como 1,500 o más sujetos, ayuda a predecir la aprobación de estos medicamentos. J Clin Epidemiol, septiembre de 2019

Aprobación acelerada de fármacos caros: una combinación problemática
29 mayo 2017
