Farmacología

Duración de la revisión regulatoria y diferencias en los tiempos de presentación de medicamentos en Estados Unidos y Europa, 2011 a 2020
17 octubre 2023
Sería beneficioso para los pacientes si se siguieran minimizando las diferencias en los tiempos de presentación entre Estados Unidos y Europa. Ann Intern Med. 17 de octubre de 2023

Validez de los desenlaces subrogados: qué dicen las evaluaciones de la FDA
27 octubre 2022
La gran mayoría de los análisis de la FDA no encontraron correlaciones sólidas entre los desenlaces sustitutos y la supervivencia general, lo que genera preocupación sobre el uso de tales resultados como criterios de valoración en los ensayos clínicos. Como la mayoría de los estudios se basaron en datos limitados, se requiere más investigación para evaluar la verdadera validez de estos resultados indirectos. Journal of Cancer Policy, diciembre de 2022.
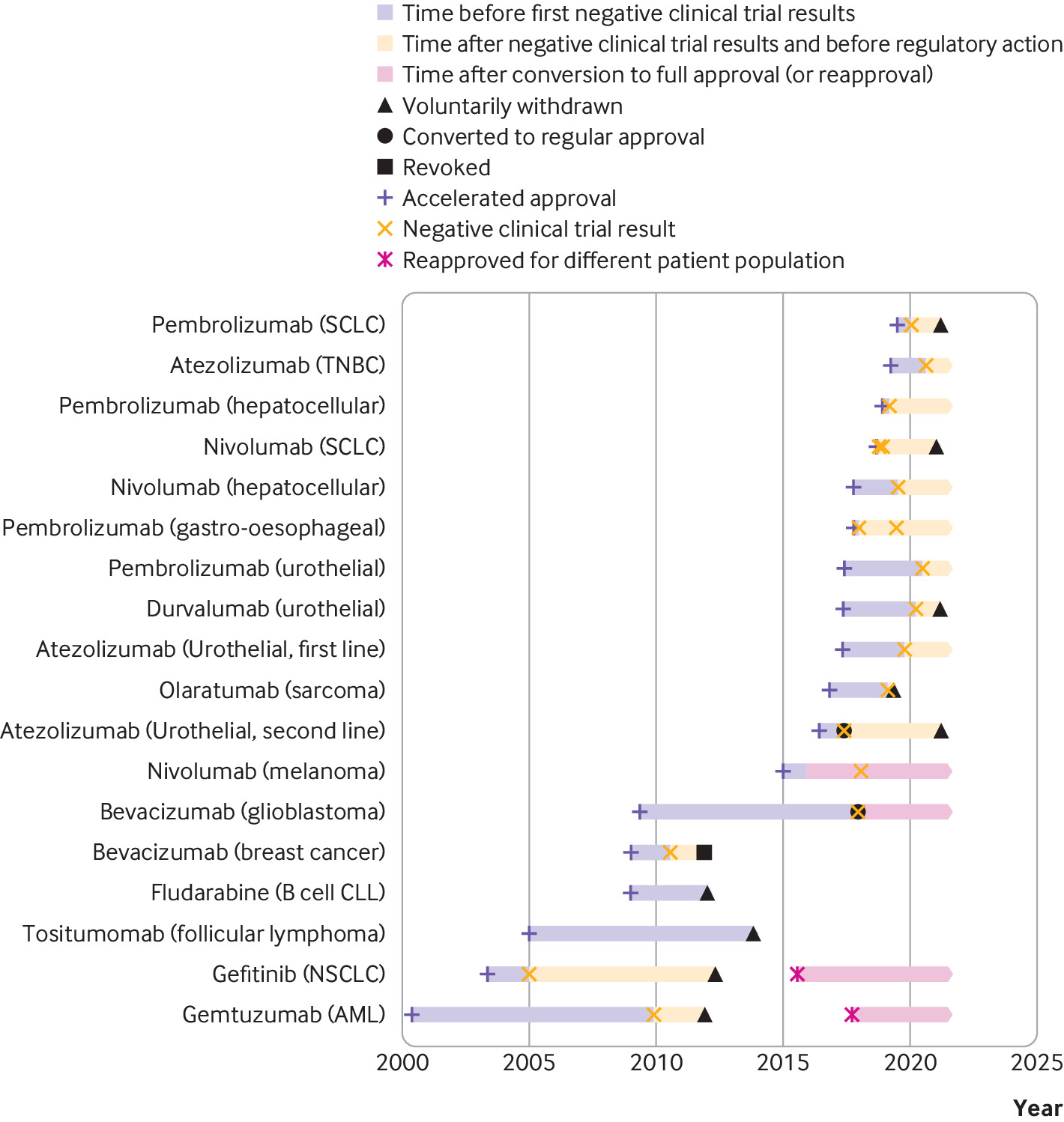
Consecuencias regulatorias y clínicas de los ensayos confirmatorios negativos de medicamentos contra el cáncer de aprobación acelerada
13 septiembre 2021
Las indicaciones de medicamentos contra el cáncer que recibieron una aprobación acelerada a menudo permanecieron en el etiquetado formal de medicamentos aprobados por la FDA y continuaron recomendándose en las guías clínicas varios años después de que los ensayos posteriores a la aprobación requeridos por ley no mostraran una mejoría en el criterio de valoración de eficacia primario. Las guías clínicas deben alinearse mejor con los resultados de los ensayos posteriores a la aprobación de medicamentos contra el cáncer que recibieron una aprobación acelerada. BMJ, 9 de septiembre de 2021

Aprobación de fármacos en base a pruebas limitadas: se hacen pocos estudios posteriores
05 mayo 2017
Cuando la FDA aprueba un fármaco en base a los resultados de un solo ensayo clínico o midiendo solamente marcadores surrogados de enfermedad se espera que los estudios post-comercialización produzcan evidencia sólida de eficacia, pero esto rara vez ocurre.BMJ, 3 de mayo de 2017

FDA: polémica por la aprobación acelerada de eteplirsen
27 septiembre 2016
