Farmacología
Efectos adversos de la vacuna Sputnik V
07 enero 2021
Luego de casi 40.000 dosis administradas en Argentina se registraron 1.088 efectos presuntamente atribuibles a la vacuna, los más frecuentes fiebre, cefalea, mialgias y molestias en el sitio de aplicación. Ministerio de Salud, 4 de enero de 2021.
Reacciones de anafilaxia por vacunas con ARNm para COVID-19
07 enero 2021
Se describen los primeros datos sobre reacciones anafilácticas por la administración de las vacunas de Pfizer-BioNTech y Moderna. Se recomienda no administrar la vacuna a personas con antecedentes de alergia severa o inmediata a cualquiera de los componentes de la vacuna, incluyendo el polietilenglicol. New England Journal of Medicine, 30 de diciembre de 2020.
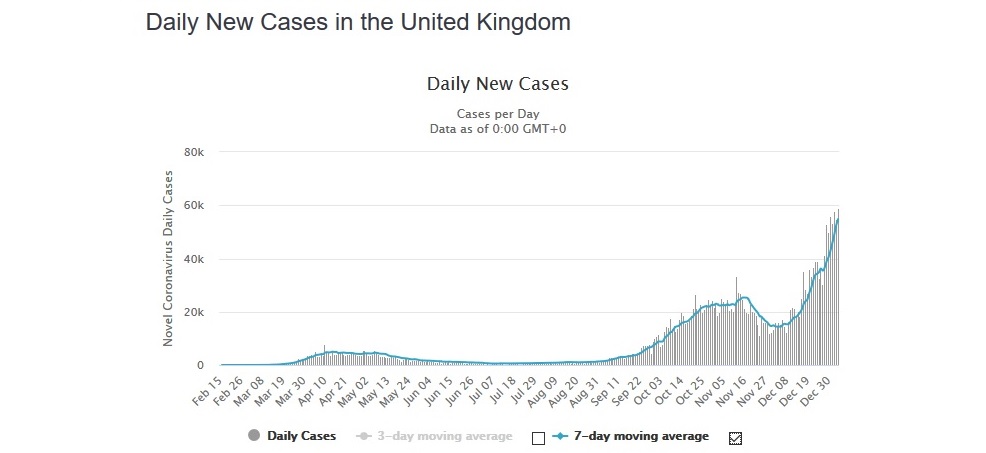
Nueva variante de SARS-CoV-2 en el Reino Unido provoca un nuevo pico de COVID-19
05 enero 2021
Aunque la nueva variante no parece ser peor que la cepa dominante previa de SARS-CoV-2 en términos de ingresos hospitalarios y mortalidad, se ha estimado que es hasta un 70% más transmisible. La esperanza para contenerla es un aumento drástico de la vacunación de los ancianos y otras personas vulnerables. The Lancet Respiratory Medicine, 5 de enero de 2021.

RACIM: Plataformas de vacunas COVID-19
05 enero 2021
En este documento, la RACIM presenta información general sobre las diferentes plataformas vacunales que se están ensayando para la COVID-19 y una tabla con los desarrollos en estudio, actualizados hasta el 29/12/2020. Red Argentina de Centros de Información de Medicamentos. 4 de enero de 2021.
Los anticuerpos específicos protegen de la reinfección con SARS-CoV-2
05 enero 2021
