Farmacología

Evaluación de los comparadores empleados en los estudios pivotales de nuevos medicamentos e indicaciones
21 marzo 2023
Aproximadamente uno de cada cuatro nuevos medicamentos o indicaciones carece de una comparación suficiente en el momento de empezar a ser utilizado en la práctica clínica. La proporción no mejora a lo largo de los últimos 10 años. Las agencias reguladoras deben ser más exigentes en la selección del comparador para los ensayos clínicos pivotales, por cuestiones éticas y sanitarias. Rev. OFIL·ILAPHAR, marzo de 2023
Variación en los costos estimados de los ensayos de beneficios clínicos pivotales que respaldan la aprobación de los nuevos agentes terapéuticos en EE. UU., 2015–2017
23 junio 2020
Los costos estimados para medir los beneficios de los nuevos agentes terapéuticosson modestos , pero aumentan exponencialmente a medida que se requieren más pacientes y visitas a la clínica para establecer un efecto farmacológico. El análisis encontró que la cantidad media de dinero gastado en ensayos clínicos es de $ 48 millones por medicamento. BMJ Open, 11 de junio de 2020
Evaluación de ensayos clínicos que respaldan la aprobación de la Administración de Alimentos y Medicamentos de los EE. UU. de nuevos agentes terapéuticos, 1995-2017
24 abril 2020
Este estudio encontró cambios en la evidencia que respalda la aprobación de nuevos medicamentos y productos biológicos por la FDA. Las aprobaciones más recientes se basaron en menos ensayos fundamentales, que, cuando se agregaron por indicación, tenían diseños menos rigurosos pero duraciones de ensayos más largas, Estos cambios sugieren que es necesario evaluar, de manera continua, la seguridad y la eficacia terapéutica después de la aprobación. JAMA Netw Open 21 de abril de 2020;
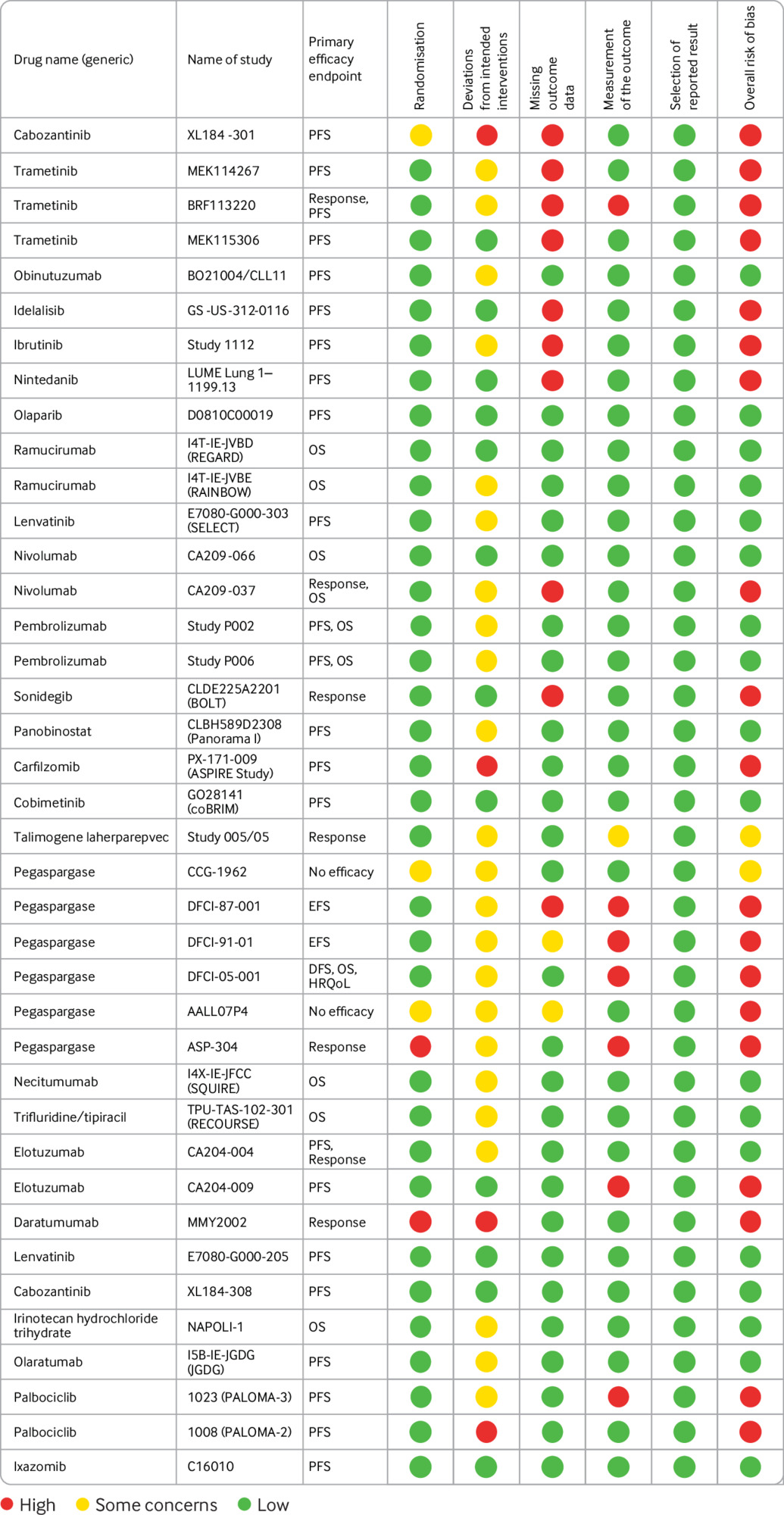
Características de diseño, riesgo de sesgo e informes de ensayos controlados aleatorios que respaldan las aprobaciones de medicamentos contra el cáncer por la Agencia Europea de Medicamentos, 2014-16
19 septiembre 2019
BMJ,18 de septiembre de 2019 La mayoría de los estudios pivotales que formaron la base de la aprobación EMA de nuevos medicamentos contra el cáncer entre 2014 y 2016 fueron ensayos controlados aleatorios. Sin embargo, se consideró que casi la mitad de ellos tenían un alto riesgo de sesgo en función de su diseño, conducta o análisis, algunos de los cuales podrían ser inevitables debido a la complejidad de los ensayos de cáncer. Los documentos reglamentarios y la literatura científica tenían lagunas en sus informes. Las publicaciones en revistas no reconocieron las limitaciones clave de la evidencia disponible identificada en los documentos reglamentarios.

Costos estimados de ensayos pivotales para nuevos agentes terapéuticos aprobados por la FDA de los EE. UU., 2015-2016
25 septiembre 2018
