Farmacología
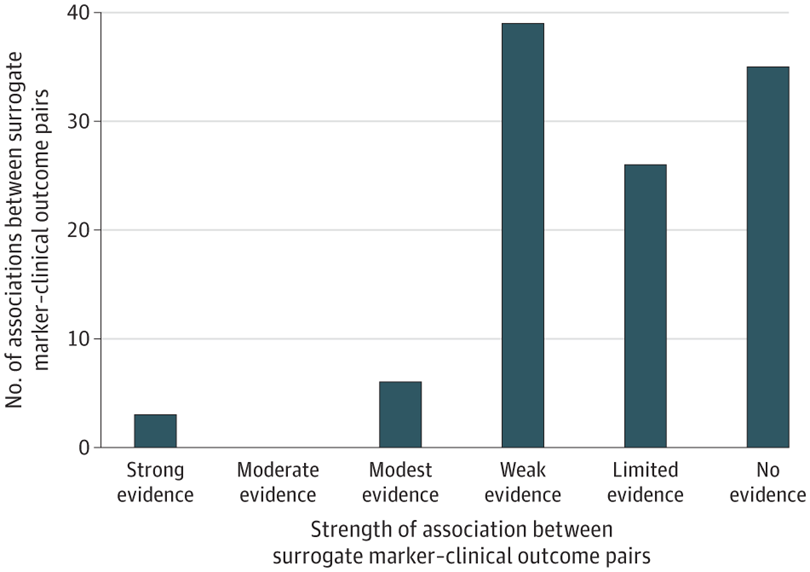
Asociaciones entre marcadores sustitutos y resultados clínicos para tratamientos de enfermedades crónicas no oncológicas
28 mayo 2024
La mayoría de las variables subrogadas utilizadas como puntos finales primarios en ensayos clínicos para respaldar la aprobación de la FDA de medicamentos para el tratamiento de enfermedades crónicas no oncológicas carecían de evidencia sólida de asociaciones con resultados clínicos de los metanálisis publicados. JAMA 22 de abril de 2024
Consecuencias globales de la aprobación acelerada de medicamentos contra el cáncer por parte de la FDA de EE. UU.
30 marzo 2022
Se han descrito previamente varios desafíos y limitaciones de esta vía para el entorno regulatorio y clínico de EE. UU. En este trabajo se discute las consecuencias que a menudo se pasan por alto de la vía de aprobación acelerada para la oncología global. Lancet Oncol, febrero de 2022

Impacto de la Unión Europea en el acceso a medicamentos en países de ingresos bajos y medianos: revisión exploratoria
12 octubre 2021
Esta revisión revela que los tomadores de decisión de la UE adoptan medidas que, a pesar de la escasa evidencia que sustenta su impacto, positivo o negativo, tienen el potencial de influir en el acceso a los medicamentos de los países de bajo y mediano ingreso (PBMI). The Lancet Regional Health – Europe, 1 de octubre de 2021

Limitaciones de los desenlaces sustitutos en la aprobación acelerada de nuevos medicamentos
17 septiembre 2021
Aunque los criterios de valoración sustitutos se utilizan ampliamente para acelerar la aprobación de nuevos fármacos, la mayoría no son predictores fiables de los resultados que más importan a los pacientes. Los reguladores sólo deben aceptar criterios de valoración sustitutos cuando no sea posible generar datos sobre los resultados clínicos. British Medical Journal, 16 de septiembre de 2021.
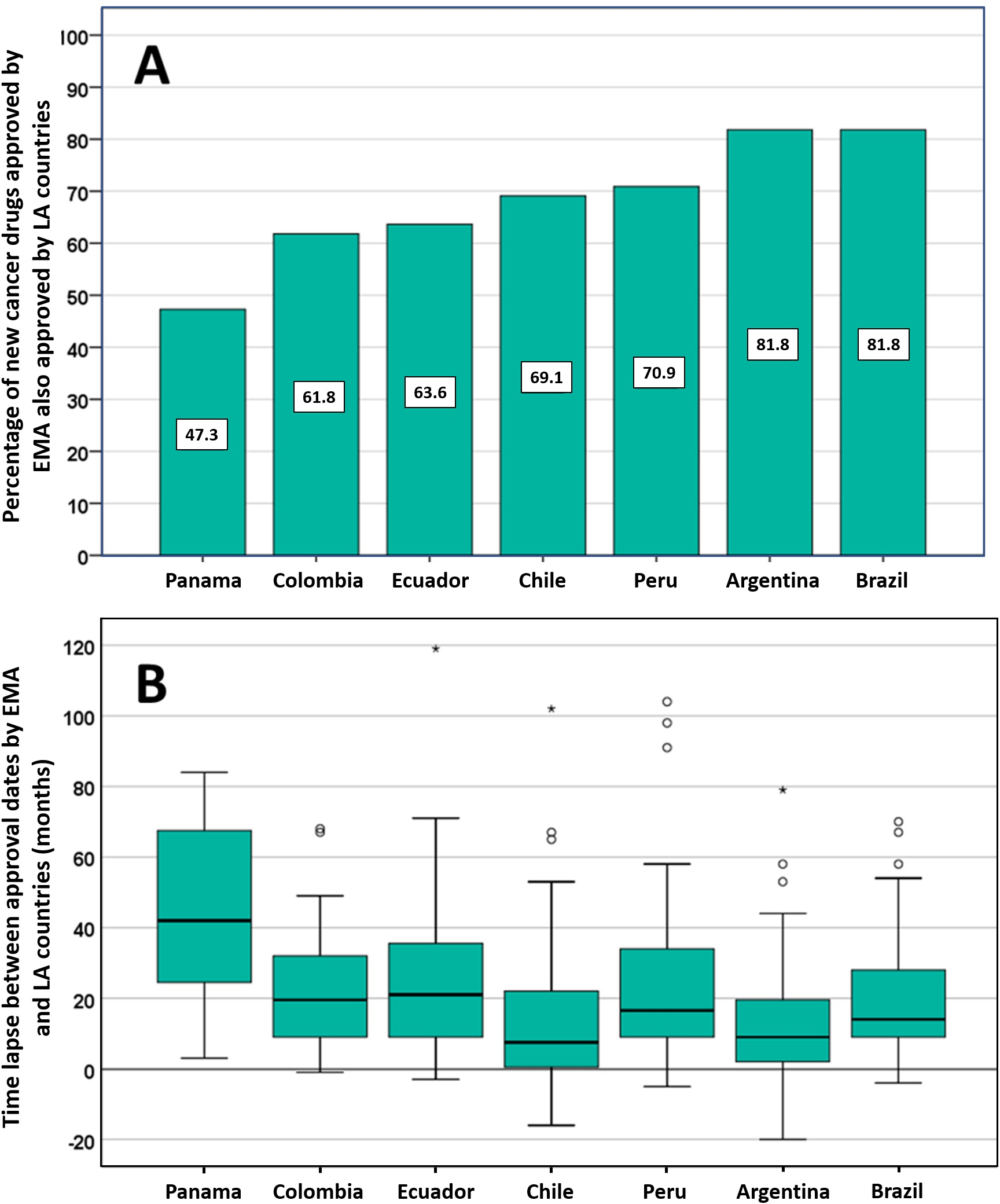
Posible impacto negativo de las decisiones de Agencias reguladoras reputadas sobre el estado de aprobación de nuevos medicamentos contra el cáncer en los países de América Latina
14 julio 2021
