Farmacología

Características, beneficio clínico y financiación de las nuevas autorizaciones de fármacos oncohematológicos en España entre 2017 y 2020
04 febrero 2025
la mayoría de los ensayos clínicos pivotales de nuevos fármacos oncohematológicos autorizados en España emplearon variables principales subrogadas y, en el momento de la autorización, pocos habían demostrado prolongar la supervivencia. Más de un tercio eran ensayos clínicos no controlados. Farm Hosp. 2024

Tiempo de revisión de los medicamentos oncológicos y sus factores subyacentes: una exploración en China
06 noviembre 2023
El breve retraso en el lanzamiento en relación con los EE. UU. fue un factor importante para la velocidad de revisión de la Administración Nacional de Productos Médicos de China, lo que podría sugerir su dependencia regulatoria latente del otro regulador global durante el período posterior a la comercialización, cuando aún faltaba nueva información sobre el beneficio clínico del medicamento. Front. Pharmacol., 1 de noviembre de 2023

Aprobaciones de biosimilares por parte de trece autoridades reguladoras: una comparación transnacional
04 septiembre 2023
En total, las jurisdicciones investigadas tuvieron de 19 a 78 biosimilares aprobados, la mayoría de ellos licenciados entre 2018 y 2020. A pesar del avance en el número de productos en los últimos años, aún persisten algunos desafíos. El acceso limitado a la información sobre la evaluación de biosimilares por parte de las Agencias Reguladoras puede afectar la confianza, lo que en última instancia puede afectar la adopción de estos productos en la práctica. Regul Toxicol Pharmacol. 31 de agosto de 2023
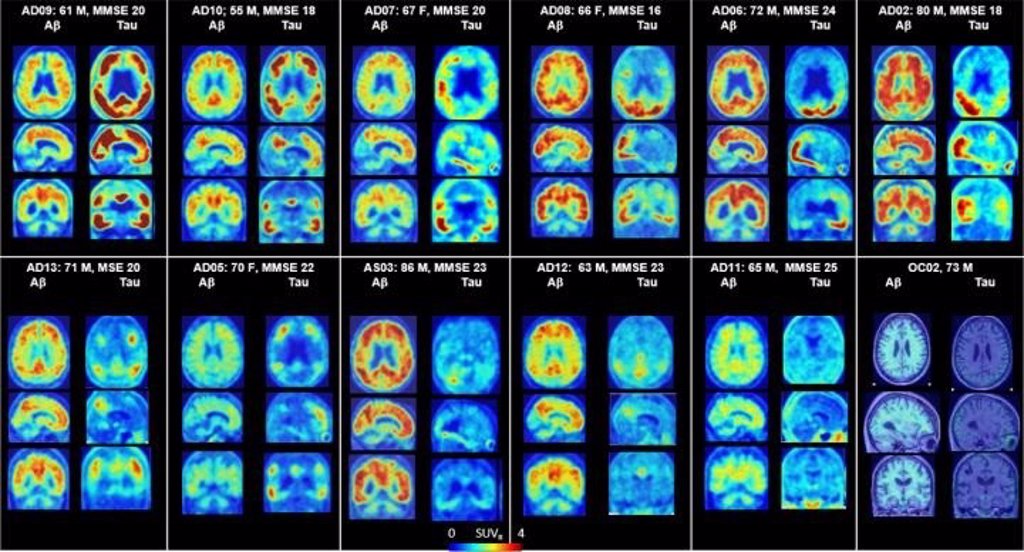
Desafíos con nuevos tratamientos para la enfermedad de Alzheimer. La aprobación acelerada de aducanumab en los Estados Unidos plantea interrogantes
14 abril 2023
Los médicos de familia suelen ser los primeros médicos en evaluar a las personas con síntomas cognitivos de EA y los primeros en recibir preguntas sobre nuevos medicamentos y posibles avances en el tratamiento. Muchos médicos ya han hecho que los pacientes pregunten sobre aducanumab. Aquí proporcionamos una descripción general de este agente y su estado actual. Can Fam Physician. marzo de 2023

Desacuerdos entre revisores regulatorios de la FDA de EE. UU. para nuevos tratamientos y acciones de seguridad posteriores a la comercialización
23 marzo 2023
