Farmacología

Debilidad de las evidencias para la aprobación acelerada de nuevos fármacos oncológicos en China
30 agosto 2023
La mayoría de los nuevos medicamentos contra el cáncer que recibieron aprobación acelerada se basaron en tasas de respuesta en estudios sin grupo de control. Las correlaciones informadas entre los criterios de valoración subrogados y la superviviencia general (SG) fueron limitadas. Nuestros hallazgos resaltan que es esencial realizar ensayos clínicos aleatorizados y medir SG o calidad de vida para garantizar los beneficios clínicos para los pacientes. eClinicalMedicine, 24 de agosto de 2023.

Retiros de medicamentos relacionados con la seguridad en China entre 1999 y 2021
15 julio 2022
La promulgación de regulaciones y el desarrollo de sistemas pasivos y activos avanzados han mejorado la farmacovigilancia en China. Se debe fortalecer la evidencia de alta calidad, la coordinación con otras autoridades reguladoras y la comunicación y el intercambio de información para optimizar la vigilancia de la seguridad de los medicamentos y la gestión de riesgos. Drug Saf 12 de julio de 2022
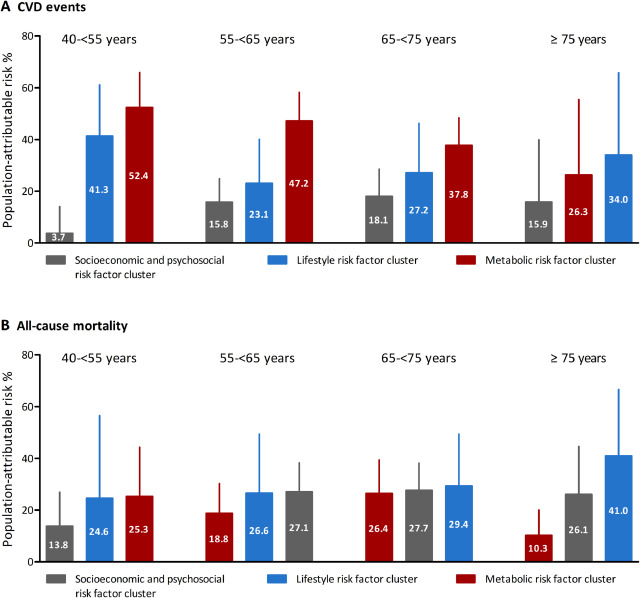
Perfiles de factores de riesgo modificables por edad para enfermedades cardiovasculares y mortalidad
29 septiembre 2021
Se identificaron perfiles de riesgo modificables específicos por edad para las enfermedades cardiovasculares y la mortalidad por todas las causas en adultos chinos, siendo la hipertensión el mayor factor de riesgo en menores de 75 años y la duración inadecuada del sueño en mayores de 75 años. Lancet Regional Health - Western Pacific, 26 de septiembre de 2021
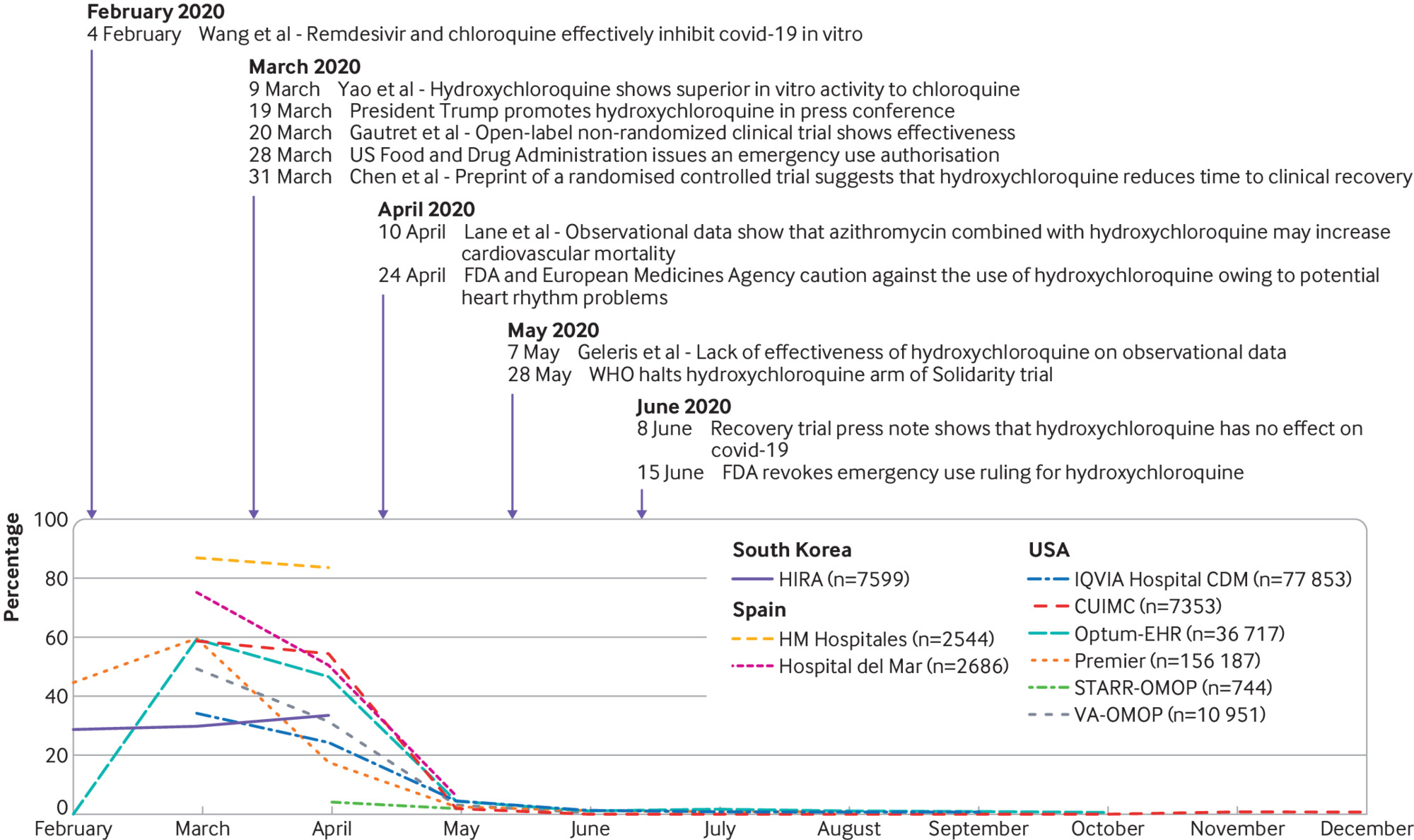
Uso de fármacos adyuvantes y reutilizados en pacientes hospitalarios con covid-19: estudio de cohorte en red multinacional
12 mayo 2021
Se utilizaron múltiples fármacos en los primeros meses de la pandemia de covid-19, con variaciones geográficas y temporales sustanciales. La hidroxicloroquina, azitromicina, lopinavir-ritonavir y umifenovir (solo en China) fueron los fármacos reutilizados más recetados. Los antitrombóticos, antibióticos, antagonistas de los receptores H2 y corticosteroides se utilizaron a menudo como tratamientos complementarios. Se necesita investigación sobre el riesgo comparativo y el beneficio de estos tratamientos en el manejo del covid-19. BMJ 11 de mayo de 2021
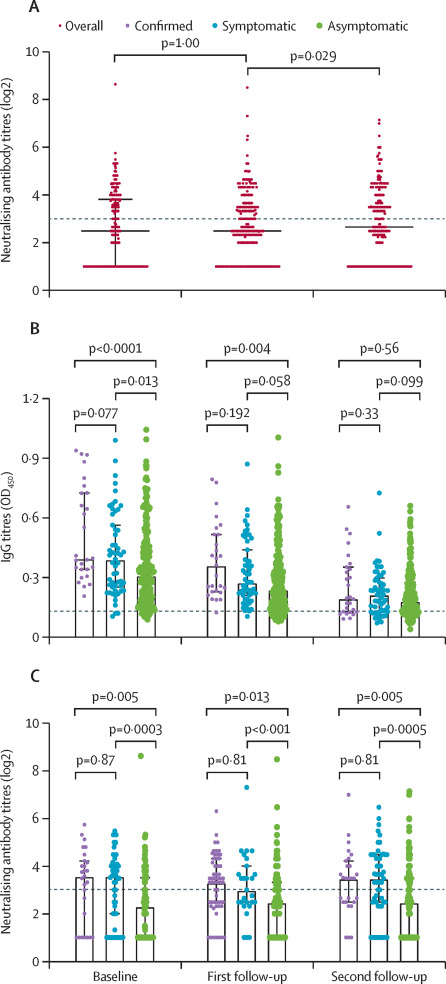
Seroprevalencia y durabilidad inmune humoral de los anticuerpos anti-SARS-CoV-2 en Wuhan, Chin
23 marzo 2021
