Farmacología

Información regional y global consolidada sobre ESAVI contra la covid-19. Décimo octavo informe. Actualización: 30 de junio de 2021
07 julio 2021
Organización Panamericana de la Salud, 6 de julio de 2021
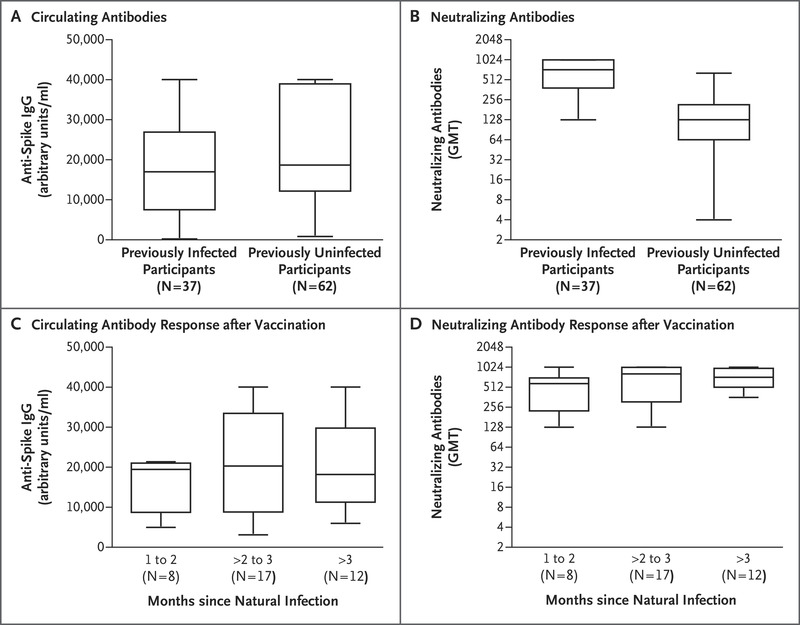
Respuesta de anticuerpos SARS-CoV-2 en personas con infección natural pasada
06 julio 2021
Los hallazgos proporcionan evidencia de que después de la administración de una sola dosis de vacuna, la respuesta humoral contra el SARS-CoV-2 en personas con antecedentes de infección por SARS-CoV-2 es mayor que la respuesta en participantes no infectados previamente que han recibido una segunda dosis. N Engl J Med, 1 de julio de 2021
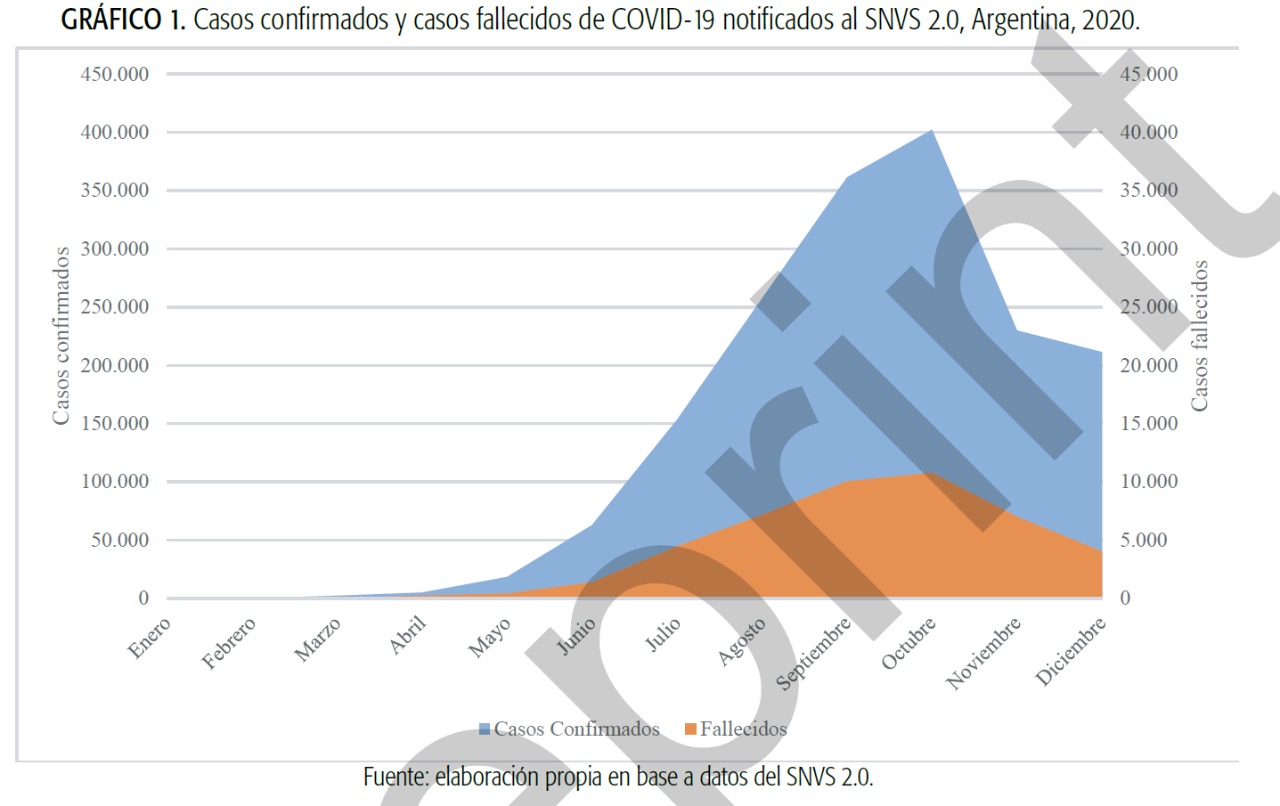
Exceso de mortalidad por todas las causas en contexto de pandemia Covid-19
06 julio 2021
Durante 2020 se registró un exceso de mortalidad por todas las causas del 10.6%. Todas esas muertes pueden ser explicadas por la pandemia, lo que pone de relevancia la robustez y sensibilidad de los registros en nuestro país. El documento publicado es un preprint y corresponde a la versión que ha sido preevaluada y aceptada por la Revista Argentina de Salud Pública para revisión por paresRev Argent Salud Publica, julio de 2021
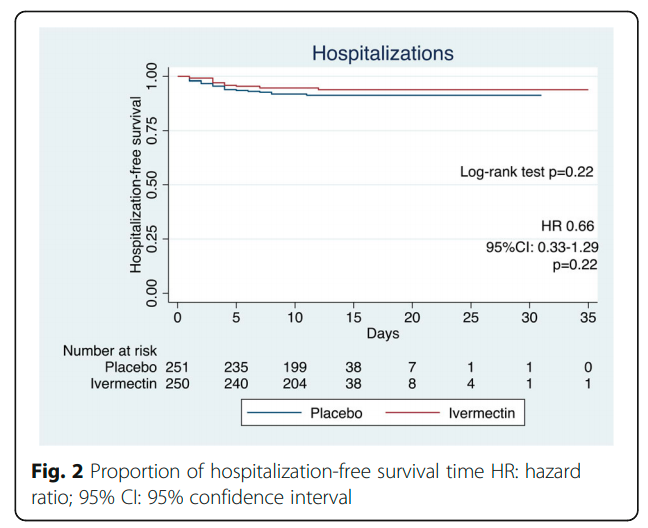
Ivermectina para prevenir hospitalizaciones en pacientes con COVID-19 (IVERCOR-COVID19) un ensayo aleatorizado, doble ciego y controlado con placebo
05 julio 2021
La ivermectina no tuvo un efecto significativo en la prevención de la hospitalización de pacientes con COVID-19. Los pacientes que recibieron ivermectina requirieron soporte ventilatorio mecánico invasivo al principio de su tratamiento. No se observaron diferencias significativas en ninguno de los otros resultados secundarios. BMC Infectious Diseases, 2 de julio de 2021
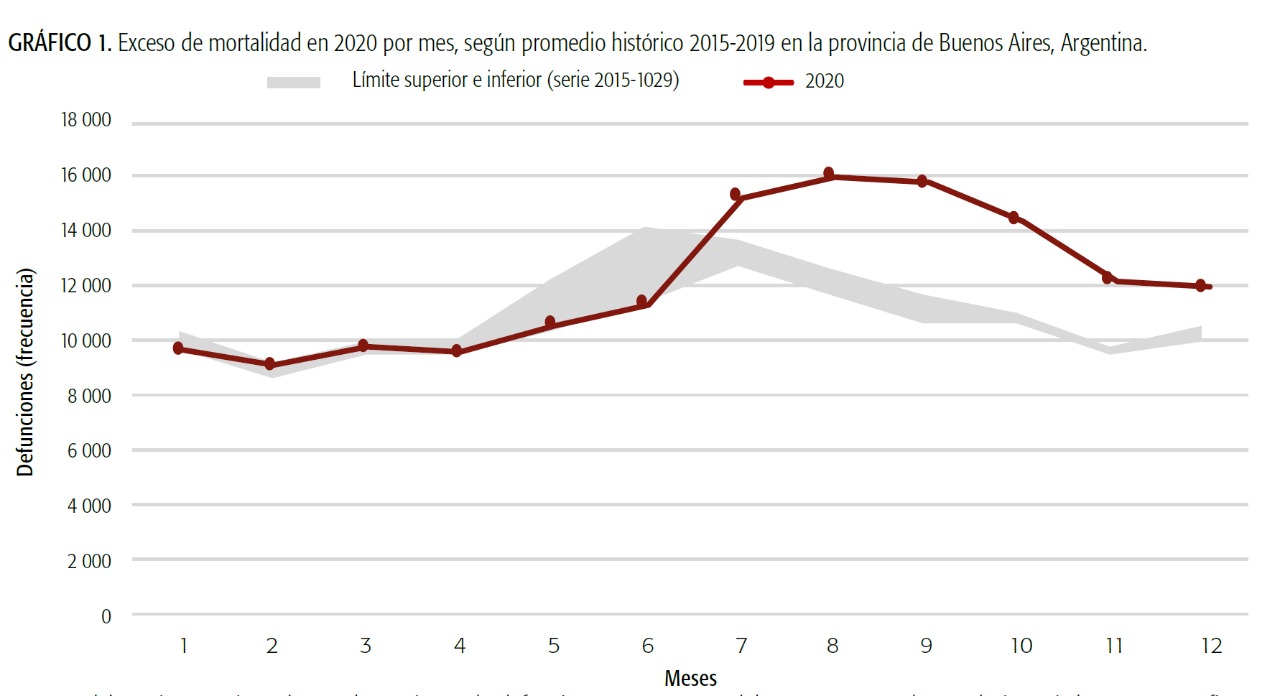
Exceso de mortalidad por la pandemia de COVID-19 durante 2020 en la provincia de Buenos Aires, Argentina.
05 julio 2021
