Farmacología
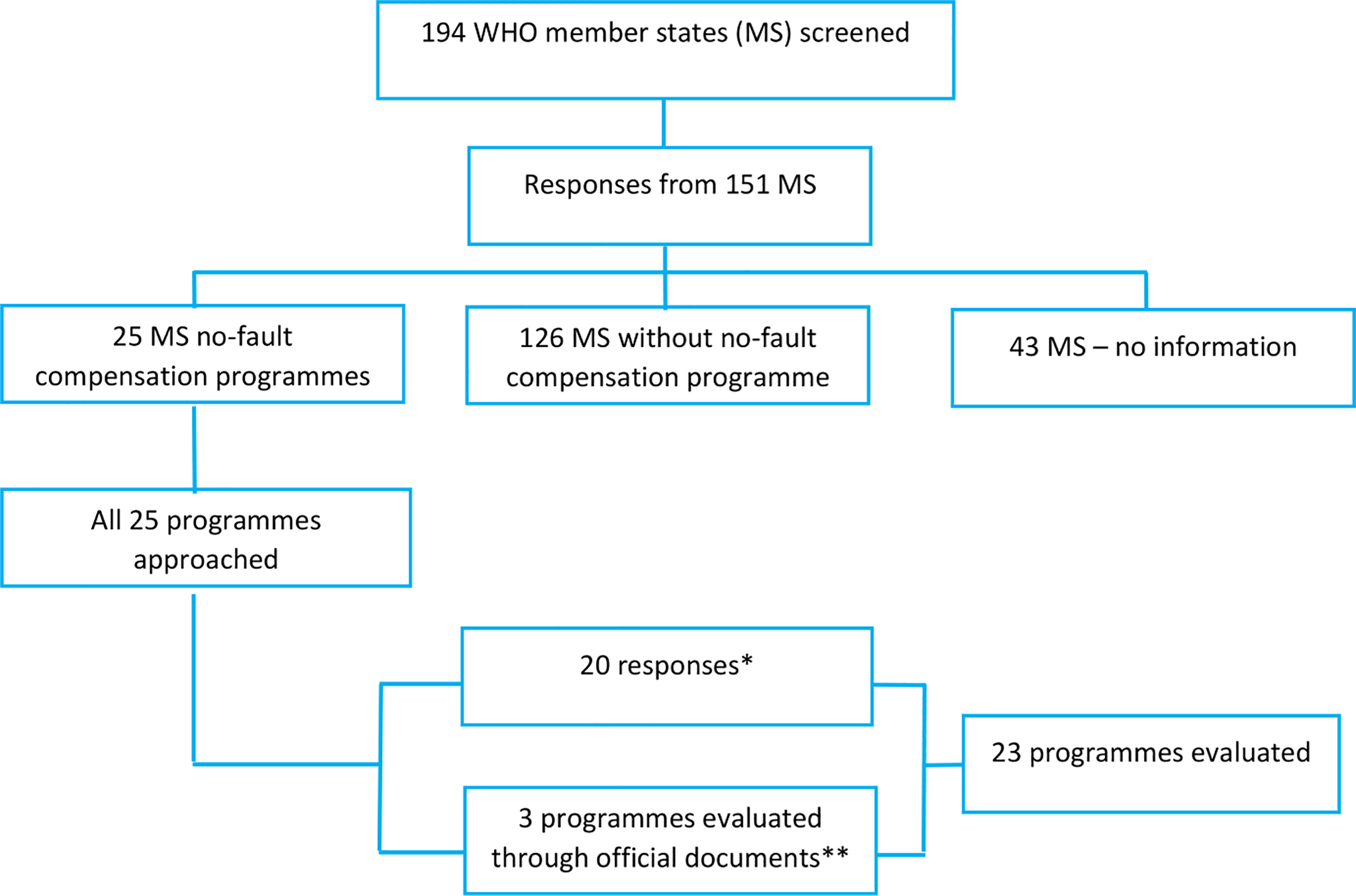
Análisis del panorama mundial de los programas de compensación sin culpa por lesiones causadas por vacunas: revisión y encuesta de los países implementadores
29 octubre 2020
Describimos las características de los sistemas de compensación sin culpa existentes durante 2018 basados en seis elementos comunes del programa. Los sistemas de compensación sin culpa por las lesiones causadas por las vacunas se han desarrollado en algunos países de ingresos altos durante más de 50 años.En la mayoría de las jurisdicciones, los reclamantes por lesiones causadas por vacunas tienen derecho a reclamar daños y perjuicios a través de un litigio civil o de un plan de compensación, pero no ambos simultáneamente. Los datos de este informe proporcionan una base empírica sobre la cual se podría desarrollar una guía global para implementar tales esquemas. PLoS ONE, 2020
Compensación sin culpa por lesiones causadas por vacunas: la otra cara del acceso equitativo a las vacunas para Covid-19
29 octubre 2020
Los autores proponen alternativas a la eximición de responsabilidad que piden los laboratorios productores de las vacunas candidatas para SARS-CoV-2, que garanticen la cobertura de los daños eventuales. Toman como modelo esquemas ya probados en situaciones similares. New England Journal of Medicine, 28 de octubre de 2020.

Popó de unicornio y aguas benditas: charlatanería COVID-19 y cartas de advertencia de la FDA
02 octubre 2020
Un pequeño porcentaje de las cartas de advertencia de la FDA se han centrado recientemente en COVID-19. Estas cartas exponen la charlatanería descarada y potencialmente dañina de los proveedores de todo el mundo que priorizan la ganancia financiera sobre la beneficencia clínica. La toma de antecedentes del paciente debe incluir consultas sobre productos no tradicionales y no aprobados para identificar, documentar e informar sobre charlatanería potencialmente dañina. Las cartas de advertencia de la FDA son un componente de una acción correctiva significativa; sin embargo, se necesita un mayor esfuerzo para difundir el conocimiento de tales productos tergiversados, no aprobados y adulterados para disuadir las compras de dichos productos. Ther Innov Regul Sci, 1 de octubre de 2020

El uso de remdesivir fuera de los ensayos clínicos durante la pandemia de COVID-19
21 septiembre 2020
Este documento tiene como objetivo revisar y analizar los enfoques regulatorios para acceder e investigar el remdesivir, comunicando la variabilidad regulatoria entre países en términos de terminología, modalidades y protocolos. J of Pharm Policy and Pract , 21 de septiembre de 2020

Los riesgos de las autorizaciones aceleradas para tratamientos en COVID-19.
14 septiembre 2020
