Farmacología
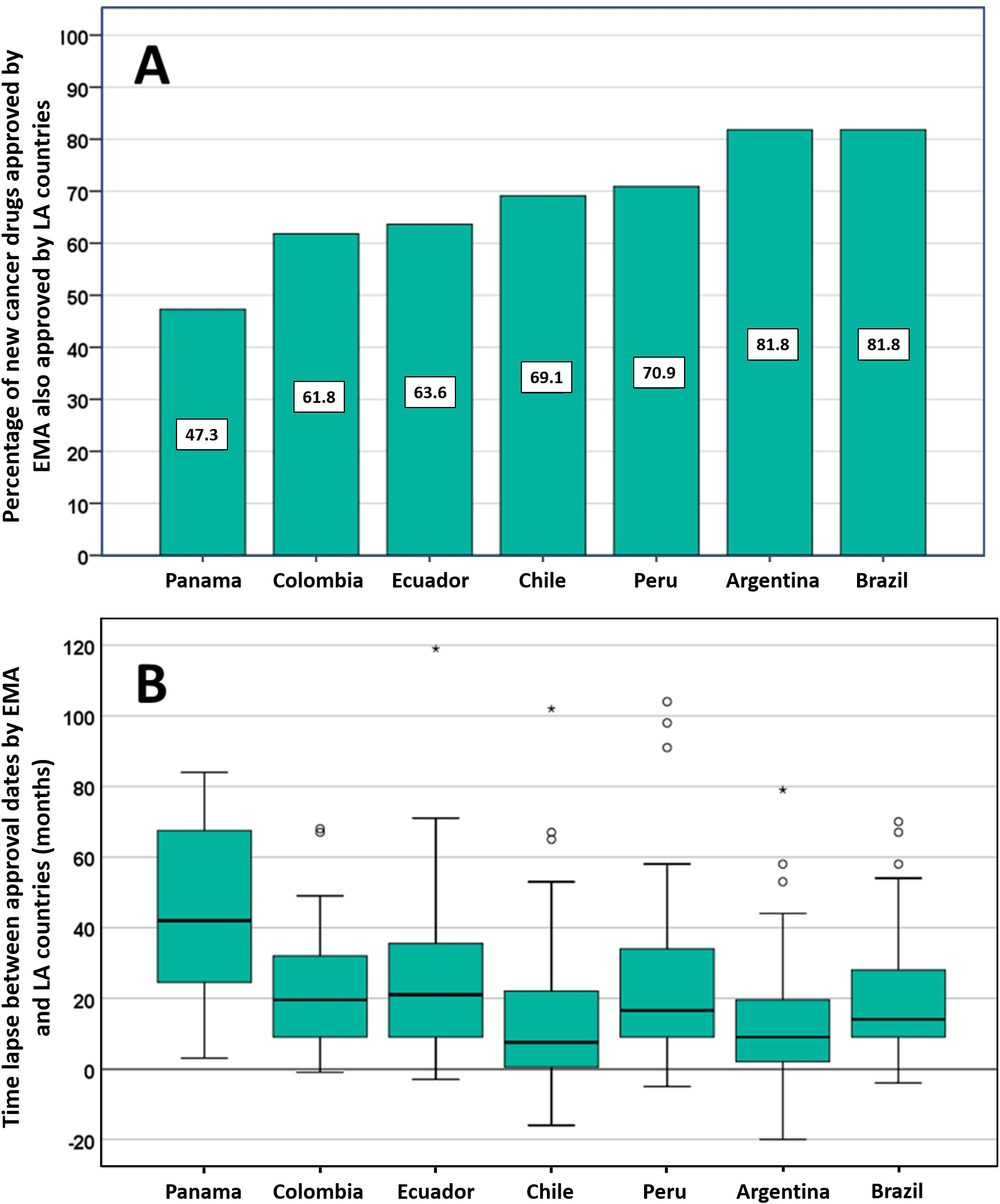
Posible impacto negativo de las decisiones de Agencias reguladoras reputadas sobre el estado de aprobación de nuevos medicamentos contra el cáncer en los países de América Latina
14 julio 2021
Los países de América Latina siguen aprobando nuevos medicamentos contra el cáncer, a menudo basándose en ensayos clínicos mal realizados que miden criterios de valoración sustitutos. La EMA y otros reguladores de renombre deben ser conscientes de que sus decisiones regulatorias pueden influir directamente en las decisiones relativas a la autorización de comercialización, los presupuestos de salud y la atención del paciente en otros lugares. PLoS ONE 13 de julio de 2021
Análisis del precio de lanzamiento y posterior a la aprobación de los medicamentos contra el cáncer, los beneficios clínicos y las implicaciones de las políticas en los EE. UU. y Europa
12 julio 2021
Durante el período de este estudio de evaluación económica, los precios de lanzamiento de los medicamentos contra el cáncer fueron sustancialmente más altos en los EE. UU. que en los países europeos de ingresos altos similares evaluados, una brecha que aumentó en los años posteriores a la aprobación. Los precios de los medicamentos contra el cáncer aumentaron con frecuencia más rápido que la inflación en los EE. UU., pero disminuyeron en términos ajustados a la inflación en Europa. Los cambios de precios no se asociaron con beneficios clínicos en ningún país. Este estudio sugiere que, EE. UU. necesitaría tomar las medidas más importantes para abordar los altos costos de los medicamentos contra el cáncer, y Europa también podría reexaminar sus regulaciones de precios para garantizar una mejor alineación con el valor clínico.JAMA Oncol. 1 de julio de 2021.
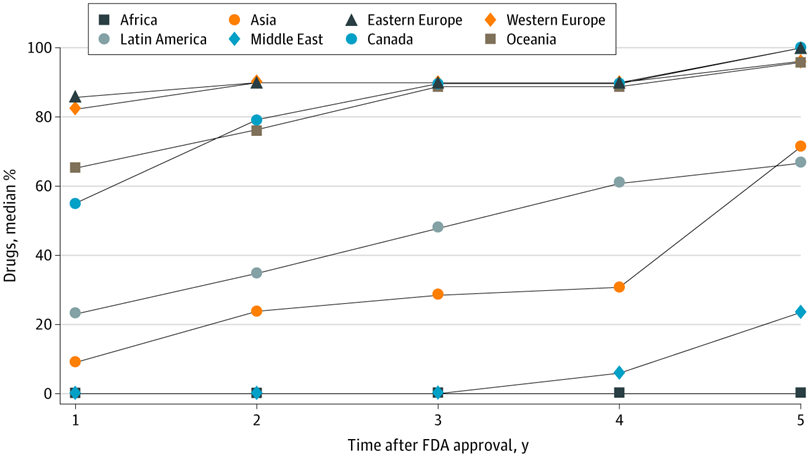
Evaluación de ensayos de medicamentos en países de ingresos altos, medianos y bajos y disponibilidad comercial local de medicamentos recientemente aprobados
17 mayo 2021
Estos hallazgos sugieren que existen brechas sustanciales entre dónde se prueban los medicamentos aprobados por la FDA y dónde finalmente están disponibles para los pacientes, lo que genera inquietudes sobre la distribución equitativa de los beneficios de la investigación a nivel de la población. JAMA Netw Open. 5 de mayo de 2021
La necesidad de distinguir las vacunas COVID-19, y los nombres genéricos
24 febrero 2021
La asignación de una Denominación común internacional (DCI) única y distinta a las sustancias activas de cada vacuna contribuiría a una prescripción segura, una distribución transnacional, una farmacovigilancia mejorada y, en última instancia, la seguridad de los receptores de la vacuna, como ocurre con las sustancias medicinales terapéuticas. Lancet 4 de febrero de 2021

La revisión integrada: la FDA moderniza la revisión de nuevas aplicaciones de comercialización de medicamentos
03 diciembre 2020
