Farmacología
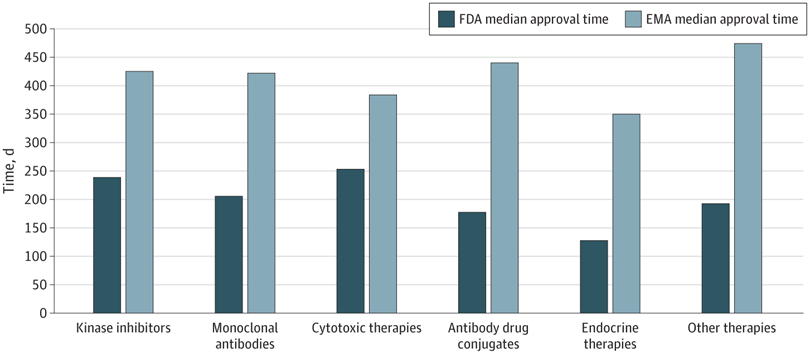
Plazos de aprobación de la terapia del cáncer, velocidad de revisión y publicación de ensayos de registro pivotales en los EE. UU. y Europa, 2010-2019
16 junio 2022
En este estudio transversal, las nuevas terapias oncológicas se aprobaron antes en EE. UU. que en Europa. La FDA recibió las solicitudes de licencia antes y tuvo tiempos de revisión más cortos. Sin embargo, se aprobaron más terapias antes de la publicación del estudio pivotal, lo que genera incertidumbre para los profesionales con respecto a la utilidad clínica y la seguridad de las terapias recientemente aprobadas. JAMA Netw Open. 10 de junio de 2022
Consecuencias globales de la aprobación acelerada de medicamentos contra el cáncer por parte de la FDA de EE. UU.
30 marzo 2022
Se han descrito previamente varios desafíos y limitaciones de esta vía para el entorno regulatorio y clínico de EE. UU. En este trabajo se discute las consecuencias que a menudo se pasan por alto de la vía de aprobación acelerada para la oncología global. Lancet Oncol, febrero de 2022

Aprobación de medicamentos por la FDA y la ética de la desesperación
29 octubre 2021
Cuando los pacientes tienen un diagnóstico de desesperación que los deja frente a una enfermedad que limita la vida sin buenas opciones de tratamiento, ¿qué papel debe desempeñar su voluntad de probar un medicamento de beneficio no probado en la toma de decisiones regulatorias? En este punto de vista, argumentamos que las voces de los pacientes deben integrarse en el proceso de aprobación de medicamentos, pero sin tal deferencia que la FDA abdique de su responsabilidad de garantizar que los medicamentos sean seguros y efectivos. JAMA Intern Med, 25 de octubre de 2021

Limitaciones de los desenlaces sustitutos en la aprobación acelerada de nuevos medicamentos
17 septiembre 2021
Aunque los criterios de valoración sustitutos se utilizan ampliamente para acelerar la aprobación de nuevos fármacos, la mayoría no son predictores fiables de los resultados que más importan a los pacientes. Los reguladores sólo deben aceptar criterios de valoración sustitutos cuando no sea posible generar datos sobre los resultados clínicos. British Medical Journal, 16 de septiembre de 2021.

¿Deberían las autoridades reguladoras aprobar medicamentos basados en desenlaces subrogados?
17 septiembre 2021
