Farmacología

Desacuerdos entre revisores regulatorios de la FDA de EE. UU. para nuevos tratamientos y acciones de seguridad posteriores a la comercialización
23 marzo 2023
Esta investigación de los desacuerdos de los revisores regulatorios y las acciones de seguridad posteriores a la comercialización entre las nuevas terapias sugiere que los desacuerdos entre los revisores regulatorios pueden conducir a importantes acciones preventivas, lo que podría mitigar la necesidad de tomar medidas de seguridad posteriores a la comercialización. BMJ Evidence-Based Medicine, 21 de marzo de 2023

Uso de pioglitazona en Australia y el Reino Unido siguiendo los avisos de seguridad de medicamentos sobre el riesgo de cáncer de vejiga
21 octubre 2022
Los resultados de este estudio de series de tiempo interrumpidas indican que las diferencias en los avisos de seguridad de Australia y el Reino Unido dieron como resultado reducciones sustanciales en el uso de pioglitazona a nivel de población en ambos países; sin embargo, no se observaron diferencias por subgrupos. Pharmacoepidemiol Drug Saf. octubre de 2022
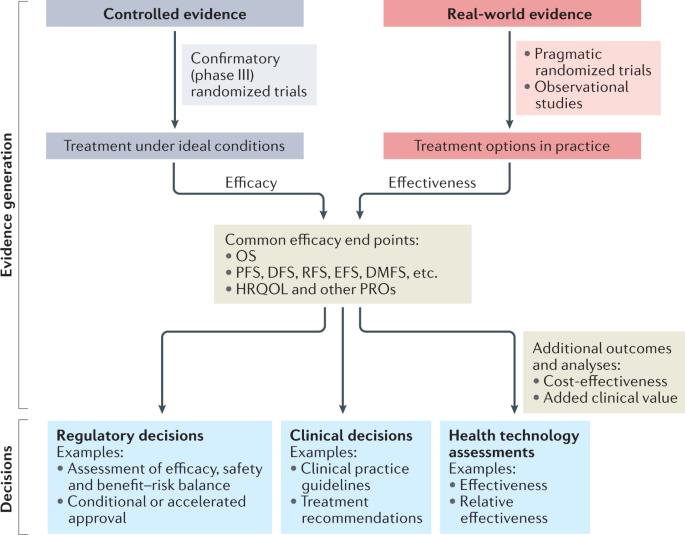
El valor de los medicamentos contra el cáncer: una visión regulatoria
20 abril 2022
Aunque es poco probable que surja una definición única que capte completamente el concepto de valor, aquí discutimos la importancia de comprender las diferentes perspectivas y cómo los reguladores pueden ayudar a informar a los diferentes tomadores de decisiones. Nat Rev Clin Oncol, marzo 2022

Regulación de la Información sobre Prescripción de Medicamentos en América Latina y el Caribe
08 abril 2022
Se evidenció un bajo nivel de armonización entre las regulaciones de estos países en cuanto al contenido y manejo (por ejemplo, si se requiere o no un prospecto físico, si está sujeto a notificación o aprobación) de la ficha técnica de los medicamentos de uso humano. Además, hay una falta visible de estandarización de los conceptos para referirse a un documento específico (por ejemplo, prospecto para profesionales de la salud, prospecto de información para el paciente e información técnica del medicamento) y en el contenido mismo. Ther Innov Regul Sci, 5 de abril de 2022

Aprobación de medicamentos por la FDA y la ética de la desesperación
29 octubre 2021
