Farmacología
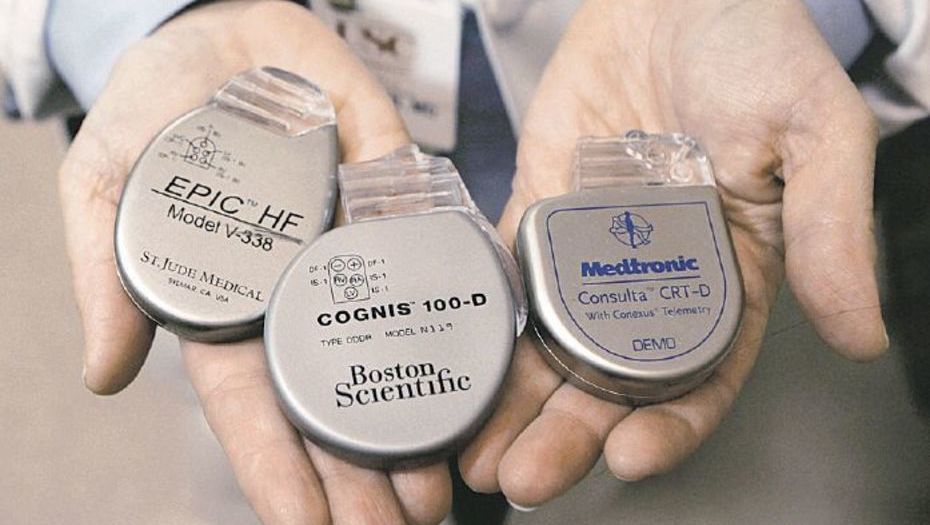
Evaluación previa a la comercialización de dispositivos médicos: un análisis transversal de estudios clínicos presentado a un comité de ética alemán
26 febrero 2019
BMJ, Open, 22 de febrero de 2019 Una gran parte de los estudios de dispositivos médicos (DM) en Alemania aplican un diseño controlado aleatorio, lo que contradice el argumento de la industria de que los ECA en los DM son comúnmente inviables.
El impacto del no enmascarar en los ensayos de medicina de cuidados intensivos
27 noviembre 2018
Jour Critical Care, diciembre 2018 Destacados • El cegamiento en los ensayos controlados aleatorios afecta el tamaño del efecto del tratamiento. • NNT para estudios ciegos es 40% más alto que para estudios no cegados. • El diseño del ensayo debe considerarse al interpretar los resultados.

Evaluación de la supervivencia libre de progresión como resultado sustituto de la calidad de vida relacionada con la salud en Oncología: revisión sistemática y análisis cuantitativo
03 octubre 2018
JAMA Intern Med, 1 de octubre de 2018. los hallazgos de esta revisión plantean preguntas sobre el supuesto de que las intervenciones que prolongan la supervivencia libre de progresión también mejoran la calidad de vida relacionada con la salud (CVRS) en pacientes con cáncer y sugieren que la CVRS se debe medir de forma directa y precisa, con un tiempo de seguimiento adecuado, en estudios futuros.

Cambios en el etiquetado y costos de los ensayos clínicos realizados bajo la Extensión de exclusividad pediátrica de la Administración de Medicamentos y Alimentos de EE. UU., De 2007 a 2012
26 septiembre 2018
JAMA Intern Med. 24 de septiembre de 2018 Los ensayos clínicos realizados bajo el programa de exclusividad pediátrica de la Administración de Medicamentosy Alimentos de EE. UU. han proporcionado información importante sobre la efectividad y la seguridad de los medicamentos utilizados en niños. Los costos para los consumidores han sido altos, superando los costos de inversión estimados para la realización de los ensayos. Como alternativa, los diseñadores de políticas deberían considerar el financiamiento directo de dichos estudios.

Seguridad del paciente y el acceso a medicamentos experimentales después de la finalización de los ensayos clínicos: regulaciones y tendencias
17 mayo 2018
