Farmacología

Boletín Fármacos: Etica, Derecho y Ensayos Clínicos
13 diciembre 2017
Boletín Fármacos, noviembre de 2017

Los tratamientos off-label no fueron consistentemente mejores o peores que los tratamientos farmacológicos aprobados en ensayos aleatorizados.
16 noviembre 2017
Journal of Clinical Epidemiology, 13 de noviembre de 2017 El estado de aprobación no indica de manera confiable qué fármacos son más favorables en situaciones con pruebas de ensayos clínicos que comparan el uso no aprobado con el aprobado. Las evaluaciones de efectividad del medicamento sin considerar el uso no indicado en la etiqueta pueden proporcionar información incompleta. Para garantizar que los pacientes reciban la mejor atención disponible, las decisiones de financiación, política, reembolso y tratamiento deben basarse en la evidencia teniendo en cuenta todo el espectro de opciones terapéuticas disponibles.

Asociación del registro de ensayos clínicos con los informes de resultados primarios en protocolos y publicaciones
14 noviembre 2017
JAMA, 7 de noviembre de 2017 Los ensayos clínicos a menudo no se registraron, no se publicaron y discreparon en el informe de los resultados primarios a través de las fuentes de información. Las limitaciones incluyen la generalización confusa más allá de la jurisdicción finlandesa y el tamaño de muestra limitado. El registro prospectivo se asoció con la publicación y publicación sin discrepancias en las publicaciones principales. Los editores de revistas, los reguladores, los comités de ética de la investigación, los financiadores y los patrocinadores deberían implementar políticas que obliguen el registro prospectivo para todos los ensayos clínicos. Solo con información accesible y completa, las intervenciones se pueden evaluar adecuadamente para la atención del paciente.
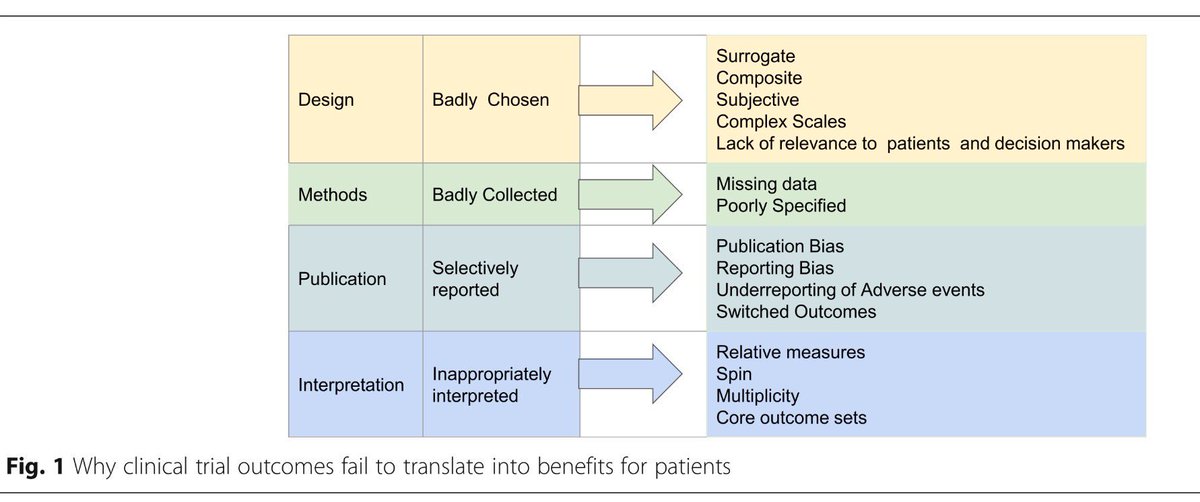
Por qué los resultados de los ensayos clínicos no se traducen en beneficios para los pacientes
28 septiembre 2017
Trials 2017 muchos ensayos continúan midiendo e informando resultados que no ayudan a mejorar la atención al paciente.. Destacamos los problemas con los resultados del ensayo que hacen difícil o imposible interpretar la evidencia y que socavan la traducción de la investigación en la práctica y la política.
Políticas de las compañías farmacéuticas sobre el acceso a los datos, resultados y métodos de los ensayos: estudio de auditoría
04 agosto 2017
