Farmacología

Diseño y diseminación de ensayos clínicos: análisis exhaustivo de clinicaltrials.gov y datos de PubMed desde 2005
08 junio 2018
BMJ, 6 de junio de 2018 El diseño del ensayo y la difusión de los resultados varían sustancialmente según el tipo y el tamaño de la institución de financiación, así como del área de la enfermedad en estudio

Seguridad del paciente y el acceso a medicamentos experimentales después de la finalización de los ensayos clínicos: regulaciones y tendencias
17 mayo 2018
Eur J Clin Pharmacol 12 de mayo de 2018 La garantía del acceso al medicamento una vez finalizado el ensayo sigue siendo obligatoria en pocos países. Teniendo en cuenta que personas consideradas vulnerables se han incluido en ensayos clínicos sin planes de acceso posterior al ensayo, los decisores deben analizar la necesidad de desarrollar normas que obliguen a garantizar el acceso posterior al ensayo clínico juicio en situaciones específicas.
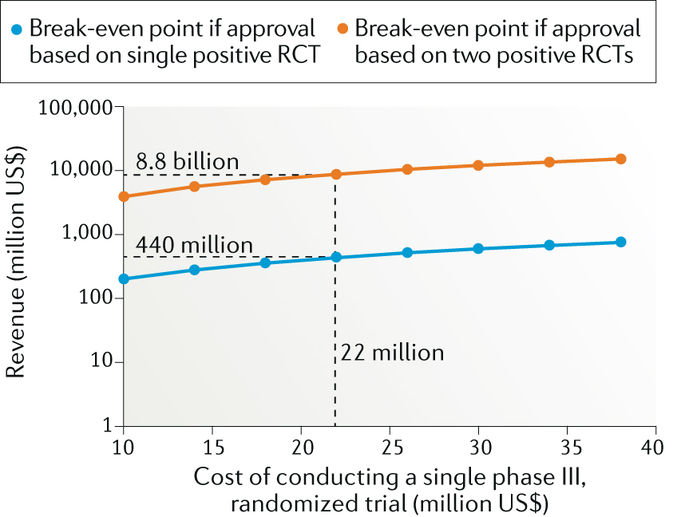
Aprobaciones de bajo valor y los elevados precios podrían incentivar un desarrollo de fármacos ineficaz
16 mayo 2018
Nat Rev Clin Oncol., 15 de mayo de 2018 La aceptación por parte de los reguladores de medicamentos, de cualquier mejora estadísticamente significativa mostrada en un único ensayo aleatorizado y los altos precios de los medicamentos han creado una situación en la que ahora, hipotéticamente, es rentable que una empresa administre una cartera de ensayos clínicos de compuestos químicamente inertes.

Medicamentos en fase de investigación: estrategias para los patrocinadores, la FDA y los sitios clínicos para prevenir los errores relacionados con el producto (Parte II)
14 mayo 2018
ISMP, 3 de mayo de 2018 Tanto para el etiquetado, empaquetamiento, como para la nomenclatura de fármacos en investigación, existen guías regulatorias limitadas, que exponen a los sitios que participan en los ensayos clínicos a muchos riesgos preocupantes de seguridad relacionados con los productos.

Problemas en la evaluación de la seguridad de los fármacos en los ensayos clínicos
07 mayo 2018
