Farmacología

La GAO (Oficina de Responsabilidad Gubernamental de Estados Unidos) identifica deficiencias en la supervisión de la FDA después de la aprobación de los fármacos
14 enero 2016
Joe Barber, First Word Pharma, 14 de enero 2016 Un informe publicado el jueves por la Oficina de Responsabilidad Gubernamental (GAO) indicó que aunque la FDA ha trabajado para acelerar la revisión de nuevos fármacos, la agencia no ha podido realizar un seguimiento adecuado de los problemas de seguridad asociados con los medicamentos, una vez aprobados. En concreto, la GAO declaró "[la] FDA carece de datos fiables y de fácil acceso sobre cuestiones de seguridad de fármacos y estudios post comercialización necesarios para cumplir con ciertos requisitos de informes responsabilidades y seguridad posterior a la comercialización y llevar a cabo un seguimiento sistemático." En su informe, la GAO señaló que según datos de la FDA, el 25 por ciento de las solicitudes de medicamentos aprobados por el Centro para la Evaluación e Investigación de Medicamentos (CDER) de la agencia, desde el 1 de octubre de 2006 al 31 de diciembre 2014, utiliza al menos un programa de revisión acelerada. El informe señaló que aunque la mayoría de las aplicaciones utilizan un solo programa, algunos utilizan dos o más, incluyendo dos solicitudes de medicamentos para oncología que se procesaron utilizando los cuatro programas de revisión acelerada.
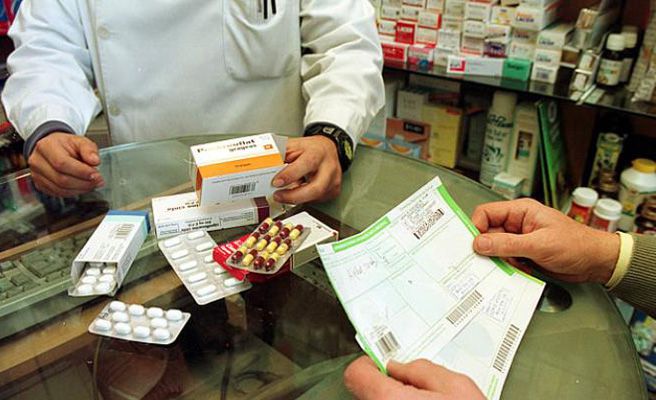
Copago en farmacia de receta en la sanidad pública española: certezas, riesgos y selección de riesgos
13 enero 2016