Farmacología
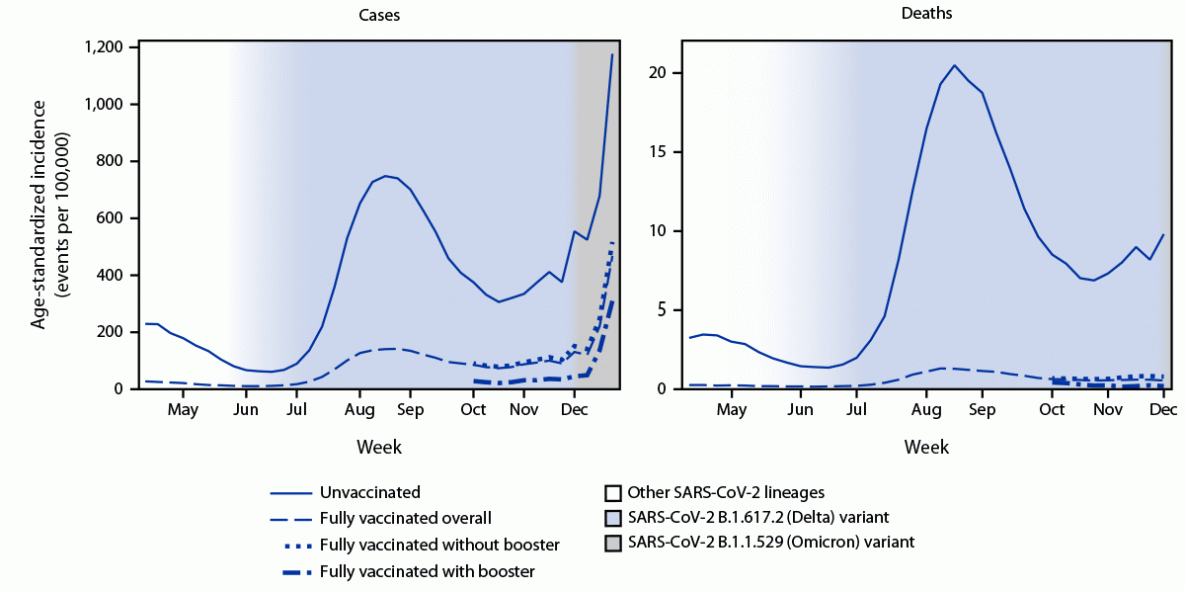
Tasas de incidencia y mortalidad de COVID-19 entre adultos no vacunados y totalmente vacunados con y sin dosis de refuerzo durante los períodos de emergencia de las variantes Delta y Omicron en EE. UU.
26 enero 2022
En 25 jurisdicciones de los EE. UU., se observaron disminuciones en las proporciones de la tasa de incidencia de casos para personas no vacunadas versus vacunas completas con y sin dosis de vacuna de refuerzo cuando surgió la variante de Omicron en diciembre de 2021. La protección contra infecciones y muerte durante el período predominante de Delta y contra infecciones durante la aparición de Omicron fueron mayores entre los receptores de la dosis de la vacuna de refuerzo, y especialmente entre las personas de 50 a 64 años y ≥65 años. CDC, 21 de enero de 2022
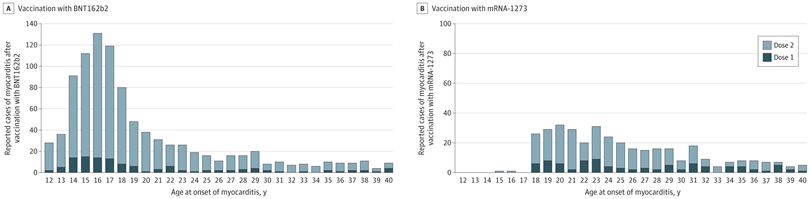
Casos de miocarditis informados después de la vacunación COVID-19 basada en ARNm en los EE. UU.
26 enero 2022
Según los informes de vigilancia pasiva en los EE. UU. entre diciembre de 2020 y agosto de 2021, el riesgo de miocarditis después de recibir vacunas COVID-19 basadas en ARNm aumentó en múltiples estratos de edad y sexo y fue más alto después de la segunda dosis de vacunación en hombres adolescentes y jóvenes. Este riesgo debe considerarse en el contexto de los beneficios de la vacunación contra la COVID-19. JAMA, 25 de enero de 2022
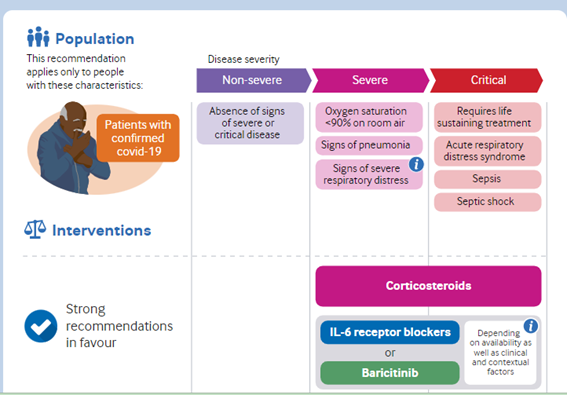
Guía viva de la OMS sobre medicamentos para covid-19: nuevas recomendaciones sobre los inhibidores de la Janus quinasa (baricitinib, ruxolitinib, tofacitinib) y sotrovimab
26 enero 2022
BMJ, 14 de enero de 2022
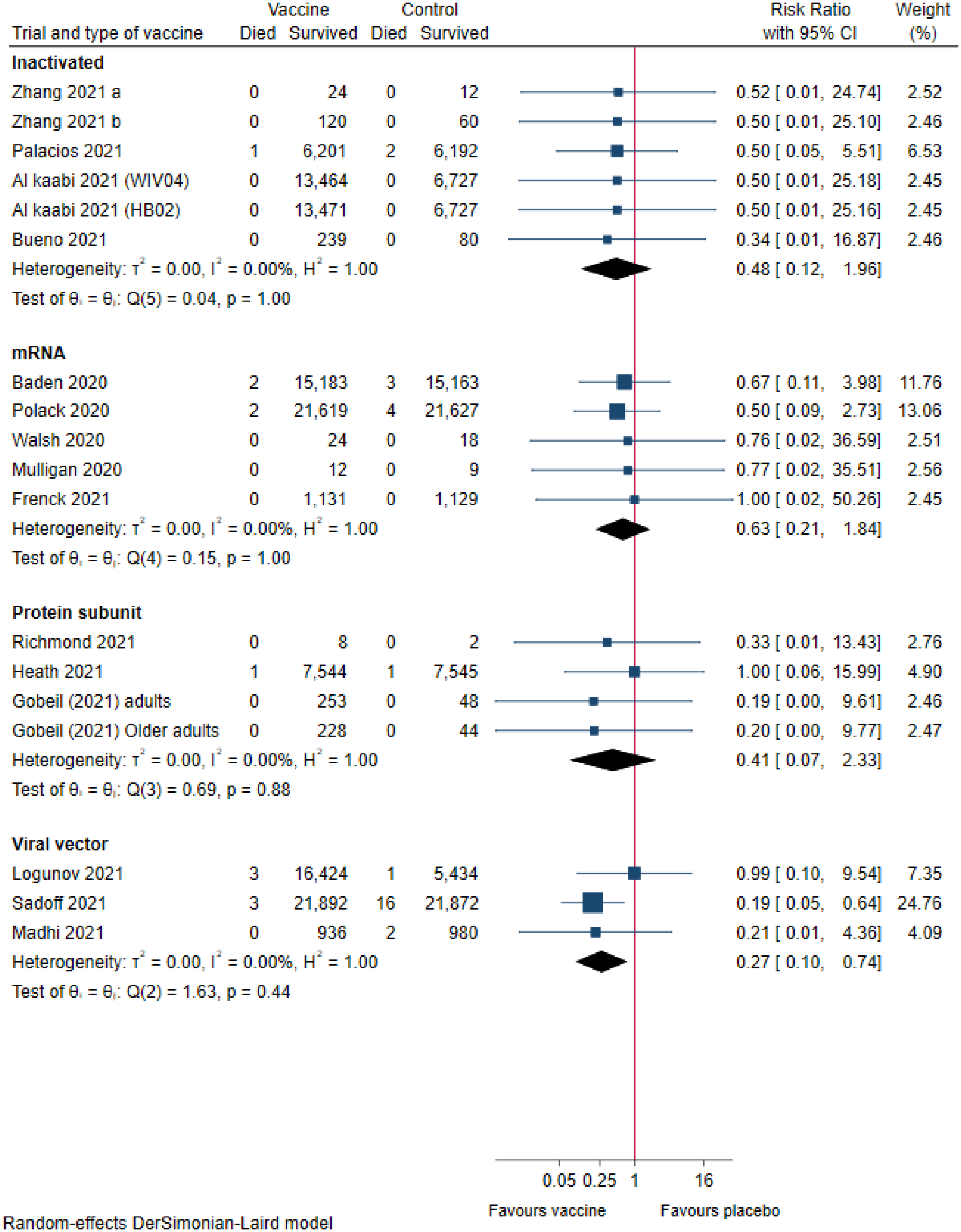
Vacunas para prevenir la COVID-19: una revisión sistemática viva con análisis secuencial de ensayos y metanálisis en red de ensayos clínicos aleatorizados
25 enero 2022
La evidencia sugiere que todas las vacunas incluidas son efectivas para prevenir el COVID-19. Las vacunas de ARNm parecen más efectivas para prevenir la COVID-19, pero las vacunas de vectores virales parecen más efectivas para reducir la mortalidad. Se necesitan más ensayos y un seguimiento más prolongado para proporcionar una mejor comprensión del perfil de seguridad de estas vacunas. PLoS ONE , 21 de enero de 2022

FDA limita el uso de ciertos anticuerpos monoclonales (bamlanivimab + etesevimab y casirivimab + imdevimab - REGEN-COV -) para tratar el COVID-19 debido a la variante Omicron
25 enero 2022
