Farmacología

Un marco para considerar el valor de la raza y la etnicidad en la estimación del riesgo de enfermedad
04 diciembre 2024
Tener en cuenta la raza y la etnicidad al estimar el riesgo de enfermedad puede mejorar la precisión de las predicciones, pero también puede fomentar una visión racializada de la medicina. Se presenta un marco de análisis de decisiones para considerar los posibles beneficios de las predicciones de riesgo que tienen en cuenta la raza frente a las que no, utilizando enfermedades cardiovasculares, cáncer de mama y cáncer de pulmón como estudios de caso. El análisis destaca la importancia de poner en primer plano los cambios en las decisiones y la utilidad a la hora de evaluar el beneficio potencial de utilizar la raza y la etnia para estimar el riesgo. Annals of Internal Medicine, 3 de diciembre de 2024.

Inteligencia artificial generativa y consideraciones éticas en la atención médica: una revisión exploratoria y una lista de verificación ética
18 septiembre 2024
La lista de verificación puede integrarse en los sistemas de revisión por pares y publicación para mejorar la investigación de la GenIA y podría ser útil para la divulgación de información relacionada con la ética de los productos impulsados por la GenIA y las aplicaciones de atención médica de dichos productos y más allá. Lancet Digit Health, 17 de septiembre de 2024

Todas las investigaciones que involucran seres humanos requieren aprobación ética
17 enero 2024
Un editorial reciente de los Archivos Argentinos de Pediatría nos recuerda que los comités de ética en investigación (CEI) son los organismos en los que la sociedad descansa la responsabilidad de velar por los intereses de los participantes en investigaciones. Llama la atención que se siga discutiendo sobre la necesidad o no de someter a la evaluación de un CEI un proyecto de investigación antes de llevarlo a cabo. Archivos Argentinos de Pediatría, diciembre de 2023.

Las estrategias de búsqueda de revisiones sistemáticas están mal informadas y no son reproducibles
05 diciembre 2023
Este estudio de metainvestigación transversal encontró que los informes de búsqueda de reseñas sistemáticas son deficientes. Para corregir esto se necesitará una respuesta multifacética por parte de los autores, revisores pares, editores de revistas y proveedores de bases de datos. Journal of Clinical Epidemiology, 3 de diciembre de 2023
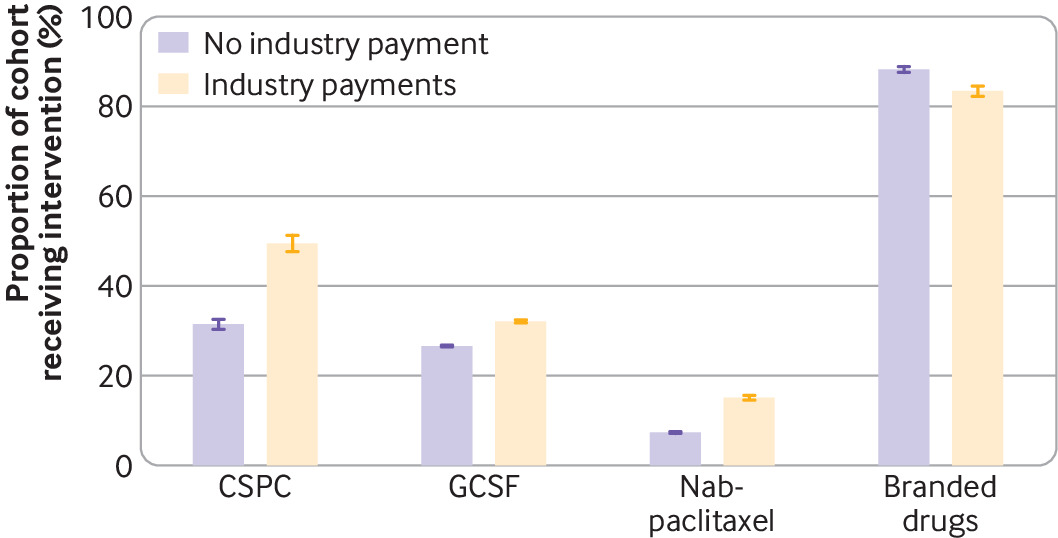
Pagos de la industria farmacéutica y entrega de medicamentos contra el cáncer no recomendados y de bajo valor
30 octubre 2023
