Farmacología
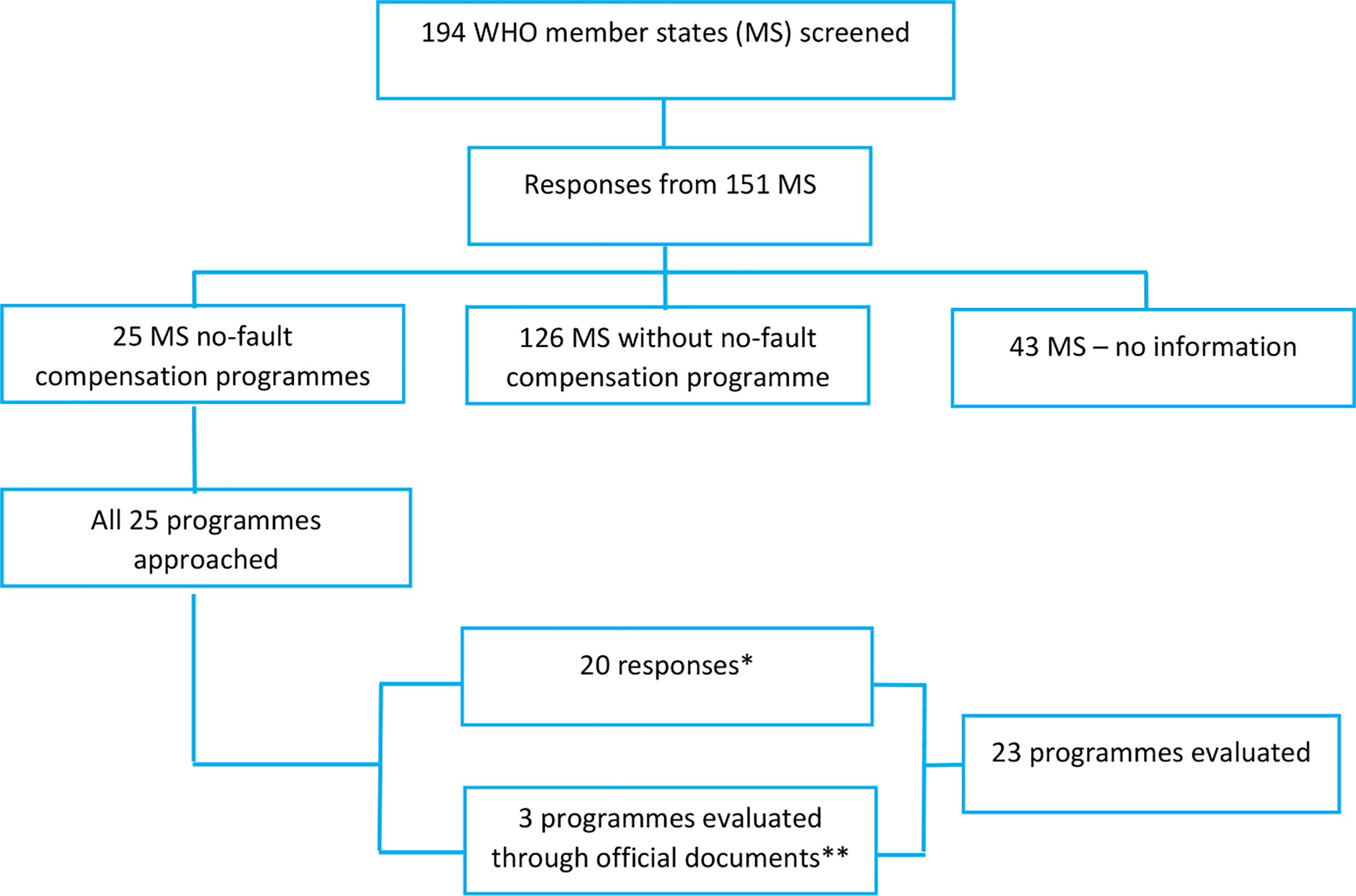
Análisis del panorama mundial de los programas de compensación sin culpa por lesiones causadas por vacunas: revisión y encuesta de los países implementadores
29 octubre 2020
Describimos las características de los sistemas de compensación sin culpa existentes durante 2018 basados en seis elementos comunes del programa. Los sistemas de compensación sin culpa por las lesiones causadas por las vacunas se han desarrollado en algunos países de ingresos altos durante más de 50 años.En la mayoría de las jurisdicciones, los reclamantes por lesiones causadas por vacunas tienen derecho a reclamar daños y perjuicios a través de un litigio civil o de un plan de compensación, pero no ambos simultáneamente. Los datos de este informe proporcionan una base empírica sobre la cual se podría desarrollar una guía global para implementar tales esquemas. PLoS ONE, 2020
Compensación sin culpa por lesiones causadas por vacunas: la otra cara del acceso equitativo a las vacunas para Covid-19
29 octubre 2020
Los autores proponen alternativas a la eximición de responsabilidad que piden los laboratorios productores de las vacunas candidatas para SARS-CoV-2, que garanticen la cobertura de los daños eventuales. Toman como modelo esquemas ya probados en situaciones similares. New England Journal of Medicine, 28 de octubre de 2020.

Uso de tramadol y otros analgésicos tras la atención de los medios de comunicación y las acciones de minimización de riesgos de los reguladores
28 octubre 2020
Este estudio de utilización de medicamentos daés a nivel nacional, identificó una disminución en el uso de tramadol coincidiendo con la atención de los medios en 2017 y continuando durante las acciones regulatorias. En general, no hubo evidencia de efectos no deseados en el uso de opioides relacionados con la atención de los medios y las acciones regulatorias. Eur J Clin Pharmacol 27 de octubre de 2020

Conceptos básicos de los Biosimilares para los pacientes
14 octubre 2020
Los biosimilares son medicamentos seguros y efectivos para el tratamiento de muchas enfermedades, tales como las enfermedades cutáneas e intestinales crónicas (como soriasis, síndrome de intestino irritable, enfermedad de Crohn y colitis), artritis, trastornos renales y cáncer. FDA, 8 de octubre de 2020
Gasto público en medicamentos huérfanos: revisión de la literatura
13 octubre 2020
