Farmacología

Lorcaserina (Belviq, Belviq XR ) FDA solicita el retiro del mercado de este fármaco para bajar de peso
20 febrero 2020
FDA, 13 de febrero de 2020 La FDA ha solicitado que el fabricante de Belviq, Belviq XR (lorcaserin) retire voluntariamente el medicamento para bajar de peso del mercado estadounidense porque un ensayo clínico de seguridad muestra una mayor incidencia de cáncer (incluidos los pancreáticos, colorrectales y pulmonares).

Clozapina: FDA fortalece la advertencia de que el estreñimiento no tratado puede conducir a problemas intestinales graves
31 enero 2020
FDA 28 de enero de 2020 Esto puede llevar a la hospitalización o incluso a la muerte si el estreñimiento no se diagnostica y trata rápidamente.

Ondansetrón: pequeño aumento del riesgo de hendiduras orales después del uso en las primeras 12 semanas de embarazo
29 enero 2020
Estudios epidemiológicos recientes sugieren que la exposición al ondansetrón durante el primer trimestre del embarazo se asocia con un pequeño aumento del riesgo de que el bebé tenga labio leporino y / o paladar hendido.Drug Safety Update 27 enero 2020

Se encontró un posible aumento del riesgo de cáncer con lorcaserina (Belviq, Belviq XR), indicada para bajar de peso, en ensayo clínico de seguridad
15 enero 2020
Al aprobar la lorcaserina, se solicitó al fabricante, que realizara un ensayo clínico aleatorizado, doble ciego, controlado con placebo para evaluar el riesgo de problemas cardiacos. En este ensayo, que se realizó en 12,000 participantes durante 5 años, más pacientes que tomaron lorcaserina fueron diagnosticados con cáncer en comparación con los pacientes que tomaron placebo, que es un tratamiento inactivo. La evaluación de esta potencial señal está en curso, y en este momento no está claro si la lorcaserina aumenta el riesgo de cáncer. FDA, 14 de enero de 2020
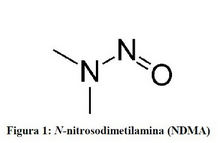
Actualización sobre las impurezas de nitrosaminas
02 enero 2020
