Farmacología
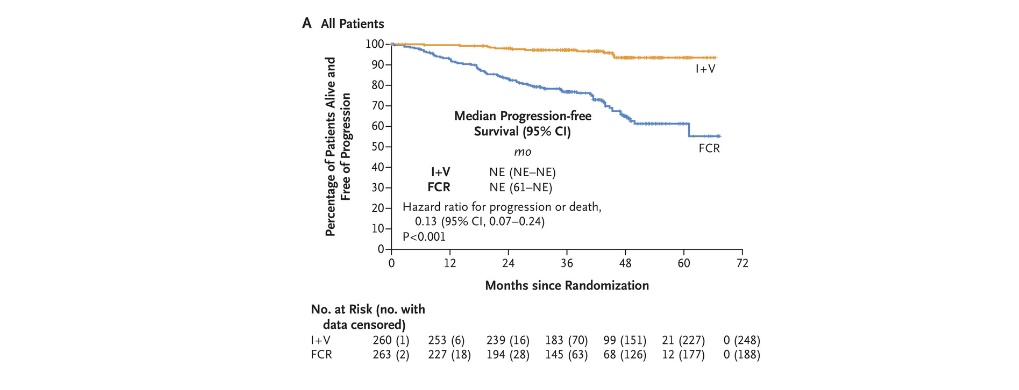
Terapia de la leucemia linfocítica crónica guiada por enfermedad residual mensurable
11 diciembre 2023
La combinación de ibrutinib-venetoclax, con dosificación guiada por la enfermedad residual mensurable, mejoró la supervivencia libre de progresión en pacientes con leucemia linfocítica crónica en comparación con el esquema de fludarabin-ciclofosfamida-rituximab. New England Journal of Medicine, 10 de diciembre de 2023.
Nuevas guías internacionales para la indicación de transfusiones de glóbulos rojos
23 noviembre 2023
Una revisión de ensayos clínicos que comparan los umbrales de transfusión más restrictivos versus los más liberales no encuentran efectos adversos de una política de transfusión más conservadora. La guía hace recomendaciones para adultos y niños en diferentes contextos clínicos. JAMA, 12 de octubre de 2023.

Enriquecimiento de condimentos y sazonadores con hierro para prevenir la anemia y mejorar la salud
19 septiembre 2023
Es incierto si el consumo de condimentos/sazonadores enriquecidos con hierro reduce la anemia, mejora la concentración de hemoglobina o mejora la concentración de ferritina. Podría reducir la deficiencia de hierro (DH). Los resultados sobre la ferritina deben interpretarse con cautela, ya que sus concentraciones aumentan durante la inflamación. El consumo de condimentos/sazonadores enriquecidos con hierro más otros micronutrientes podría reducir la anemia, y no se sabe con certeza si mejorará la concentración de hemoglobina o de ferritina. Cochrane Database Syst Rev, 1 de septiembre de 2023
Riesgo de tromboembolismo venoso recurrente al interrumpir la anticoagulación en pacientes con trombosis asociada al cáncer
11 septiembre 2023
Este metanálisis demuestra una alta tasa de trromboembolismo venoso ecurrente después de la interrupción del tratamiento anticoagulante en pacientes con trombosis asociada al cáncer. Nuestros resultados respaldan las guías clínicas actuales para continuar la anticoagulación en pacientes con cáncer activo. eClinicalMedicine, 8 de septiembre de 2023.
Tromboembolismo venoso con uso de anticonceptivos hormonales y antiinflamatorios no esteroides
07 septiembre 2023
