Farmacología

Metformina para niños y adolescentes con sobrepeso y obesidad con trastornos del espectro bipolar y trastornos del estado de ánimo relacionados tratados con antipsicóticos de segunda generación
13 noviembre 2025
Aunque su efecto sobre el peso es modesto, concluimos que, para la mayoría de los pacientes, los beneficios de la metformina superan los riesgos. Los resultados de este ensayo pragmático sugieren que los médicos deberían considerar la prescripción de metformina para jóvenes con trastorno bipolar y trastornos del estado de ánimo relacionados que presentan sobrepeso u obesidad y que reciben tratamiento con antipsicóticos de segunda generación. Lancet Psychiatry. 12 de noviembre de 2025
Tratamiento de la fibrilación auricular en pacientes con stents liberadores de fármacos
13 noviembre 2025
En pacientes con fibrilación auricular a quienes se les había implantado un stent liberador de fármacos al menos un año antes, la monoterapia con anticoagulantes orales de acción directa (ACOD) no fue inferior a la terapia combinada en cuanto a eventos clínicos adversos netos. N Engl J Med. 8 de noviembre de 2025
Factores predictivos de la aceptación y la puntualidad de la vacunación infantil en una población urbana diversa
13 noviembre 2025
Los diferentes factores predictivos de la cobertura y la puntualidad de la vacunación ponen de manifiesto la necesidad de estrategias que aborden tanto el acceso como la administración oportuna. Los datos locales deben fundamentar las intervenciones específicas y adaptadas a cada lugar. Se recomiendan servicios culturalmente competentes, integrados en la atención primaria de rutina y diseñados conjuntamente con las comunidades. British Journal of General Practice , 11 de noviembre de 2025
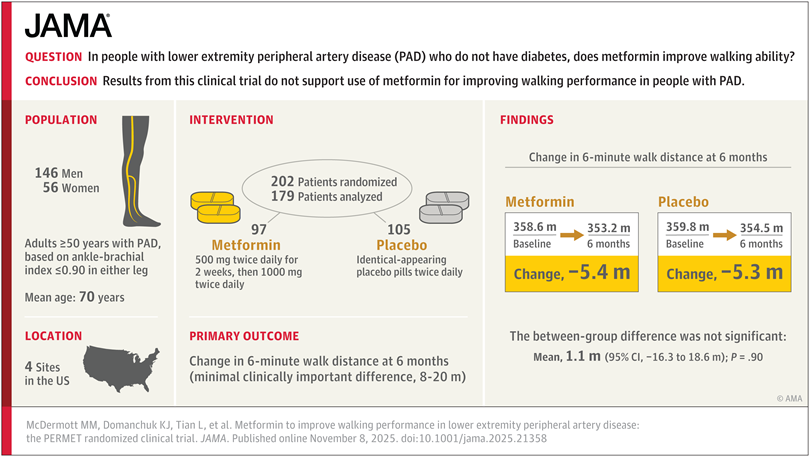
Metformina y rendimiento al caminar en pacientes con enfermedad arterial periférica. Ensayo PERMET
13 noviembre 2025
En personas con enfermedad arterial periférica (EAP) sin diabetes, la metformina no mejoró la distancia recorrida en la prueba de marcha de 6 minutos a los 6 meses de seguimiento, en comparación con el placebo. Estos resultados no respaldan el uso de metformina para mejorar el rendimiento al caminar en pacientes con EAP. JAMA 8 de noviembre de 2025

Participación de pacientes y público en los comités de evaluación de tecnologías sanitarias: ¿quién está libre de conflictos de interés?
13 noviembre 2025
