Farmacología
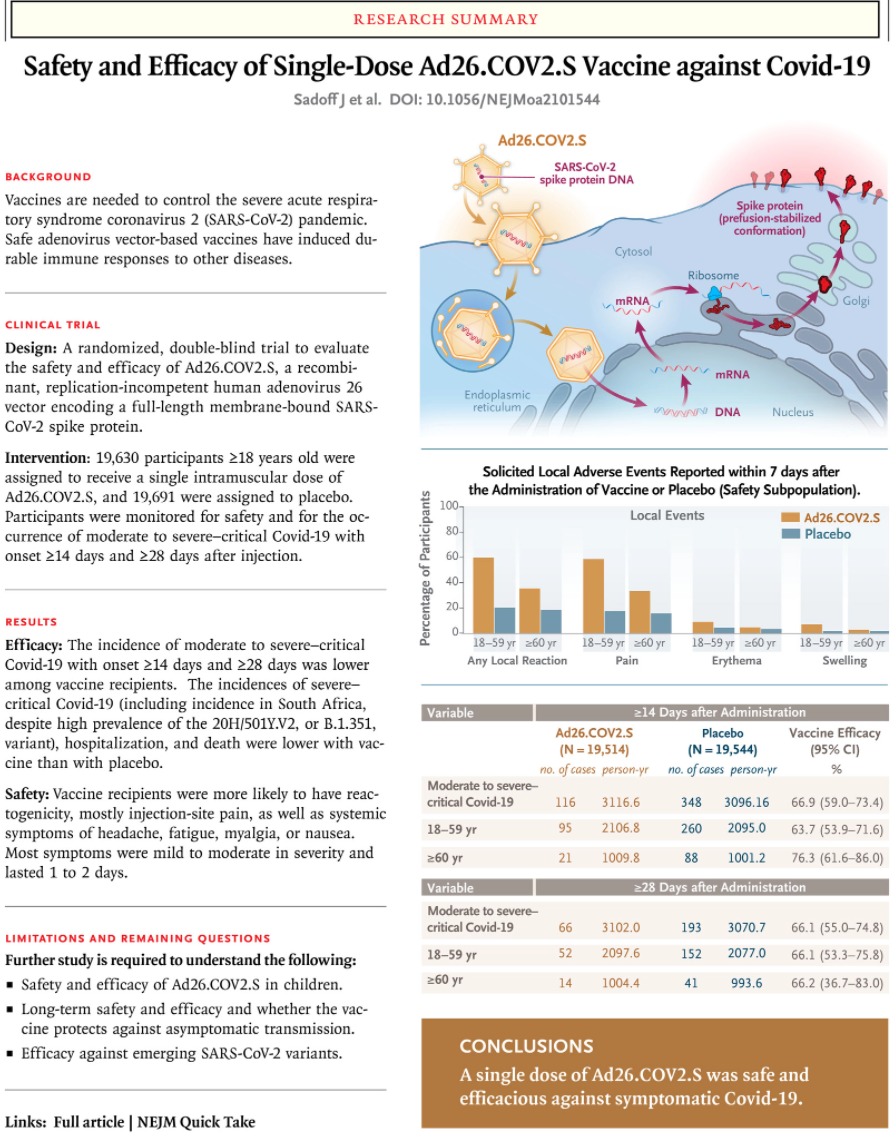
Seguridad y eficacia de la vacuna Ad26.COV2.S de dosis única (Janssen) contra Covid-19
22 abril 2021
Una dosis única de Ad26.COV2.S protegió contra la infección sintomática por Covid-19 y asintomática por SARS-CoV-2 y fue eficaz contra la enfermedad grave, incluyendo la hospitalización y la muerte. La seguridad pareció ser similar a la de otros ensayos de fase 3 de las vacunas Covid-19. N Eng J Med, 21 de abril de 2021

Tratamiento antiplaquetario oral después del síndrome coronario agudo
21 abril 2021
La terapia antiplaquetaria dual reduce las tasas de eventos cardiovasculares en pacientes con síndrome coronario agudo. Las combinaciones específicas y la duración de la terapia antiplaquetaria doble deben basarse en las características del paciente: riesgo de isquemia miocárdica hemorrágica. JAMA, 20 de abril de 2021

Guías para el manejo del síndrome trombótico postadministración de vacunas contra la COVID-19 y de los antecedentes de Síndrome de Guillain Barré. Informe especial Comisión Nacional de Seguridad en Vacunas
21 abril 2021
Comisión Nacional de Seguridad en Vacunas (CoNaSeVa) | Ministerio de Salud. Abril 2021.
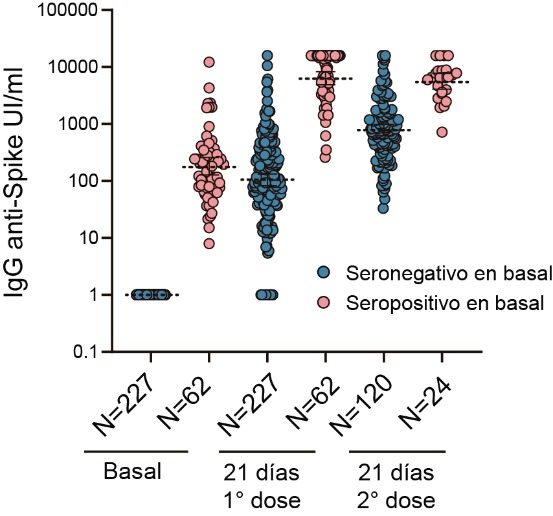
Empleo de la vacuna Sputnik V en Argentina: Evaluación de respuesta humoral frente a la vacunación. Informe Final Enero‐Marzo 2021.
21 abril 2021
El trabajo mostró que el 94% de las personas que recibieron una sola dosis y el 100% con dos dosis de la vacuna producen anticuerpos específicos. Además las personas previamente infectadas que recibieron solo una dosis producen cinco veces más anticuerpos que quienes completaron el esquema de dos dosis sin antecedente de COVID-19. Ministerio de Salud de la Provincia de Buenos Aires, Ministerio de Ciencia, Tecnología e Innovación,-Instituto Leloir‐ CONICET‐INBIRS‐UNLP. 13 de Abril de 2021
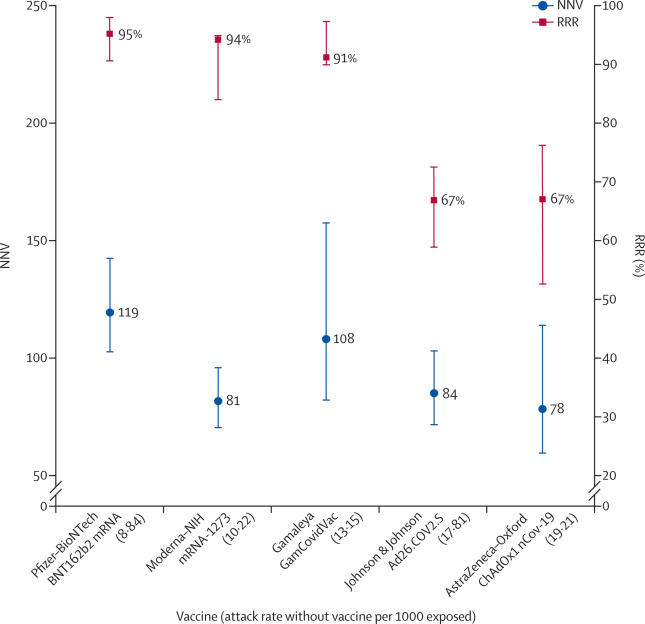
Eficacia y efectividad de la vacuna COVID-19: el elefante (no) en la habitación
21 abril 2021
